题目内容
5.将两个铂电极插人KOH溶液中,向两极分别通人CH4和O2,构成甲烷燃料电池.已知.通入CH4的一极,其电极反应式是:CH4+10OH--8e-═CO32-+7H2O;另一极通入O2.下列叙述不正确的是( )| A. | 通人CH4的电极为负极 | |
| B. | 正极发生氧化反应 | |
| C. | 燃料电池工作时,溶液中的OH-向负极移动 | |
| D. | 该电池使用一段时间后应补充KOH |
分析 燃料原电池中,甲烷失电子发生氧化反应,所以通入燃料的电极为负极,电池反应式为:CH4+10 OH--8e-═CO32-+7H2O,通入氧化剂的电极为正极,其电极反应是:O2+2H2O+4e-═4OH-,总反应为:CH4+2OH-+2O2=CO32-+3H2O;溶液中阴离子流向负极,阳离子流向正极,据此进行解答.
解答 解:A.甲烷失电子发生氧化反应,所以通入燃料的电极为负极,故A正确;
B.原电池的正极上得到电子发生还原反应,故B错误;
C.溶液中阴离子流向负极,阳离子流向正极,则氢氧根离子向负极移动,故C正确;
D.该原电池的总反应为:CH4+2O2+2OH-=CO32-+3H2O,所以该电池使用一段时间后应补充KOH,故D正确;
故选B.
点评 本题考查碱性甲烷电池的工作原理,题目难度不大,注意掌握电极反应式的书写方法,正确判断两极发生的反应为解答关键,在学习中注意归纳电子、电流、离子的流向,试题培养了学生的分析能力及灵活应用能力.

练习册系列答案
 全能测控期末小状元系列答案
全能测控期末小状元系列答案 智趣暑假温故知新系列答案
智趣暑假温故知新系列答案
相关题目
13.一种新型燃料电池,一极通入空气.另一极通入甲烷气体;电解质是掺杂氧化钇化锆(ZrO2)晶体,在熔融状态下能传导O2-,下列对该燃料电池说法正确的是( )
| A. | 在熔融电解质中,O2-由负极移向正极 | |
| B. | 通入空气的一极是正极,电极反应为:O2+2H2O+4e-═4OH- | |
| C. | 通入甲烷的一极是负极,电极反应为:CH4+8e-+4O2-═CO2+2H2O | |
| D. | 当电路中通过amol电子时,理论上能生成标准状况下CO2气体2.8aL |
16.反应2SO2+O2?2SO3达到平衡后,再向反应器中充入由18O组成的氧气,经一段时间后,18O可能存在于( )
| A. | 生成的SO3中 | B. | O2和SO3中 | C. | 剩余的SO3中 | D. | O2、SO2和SO3中 |
13.某化合物XY2的Y-的粒子结构示意图可能是( )
| A. | 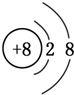 | B. | 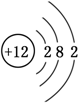 | C. | 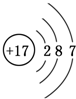 | D. | 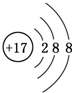 |
10.下列叙述中,与胶体性质无直接关系的是( )
| A. | 含有少量硫的酒精溶液,加入大量水后形成乳白色液体,用滤纸过滤不能分离出硫 | |
| B. | 原硅酸溶液中加入硫酸铵饱和溶液,结果产生沉淀 | |
| C. | 硫酸铜溶液中加入硫化钠溶液产生黑色沉淀 | |
| D. | 用水稀释牛奶,用一束强光照射,从侧面观察,可以看到一条清晰的光路 |
17.下列物质之间的相互关系不正确的是( )
| A. | 酸性:HClO4>H2SO4>H3PO4>H2SiO3 | B. | O2和O3互为同素异形体 | ||
| C. | H、D、T互为同位素 | D. | 干冰和冰为同一种物质 |
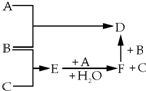 有A、B、C三种常见单质,其有关反应如图所示:已知B、E的水溶液显酸性,E在一定条件下有还原性,但不能被浓H2SO4氧化,B显黄绿色,D遇KSCN溶液显血 红色.
有A、B、C三种常见单质,其有关反应如图所示:已知B、E的水溶液显酸性,E在一定条件下有还原性,但不能被浓H2SO4氧化,B显黄绿色,D遇KSCN溶液显血 红色.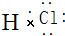 ;
;