题目内容
水溶液中能大量共存的一组离子是( )
| A、Na+、Ca2+、Cl-、SO42- |
| B、Mg2+、NH4+、Cl-、SO42- |
| C、Fe2+、H+、SO32-、ClO- |
| D、K+、Fe3+、NO3-、SCN- |
考点:离子共存问题
专题:离子反应专题
分析:离子之间不反应生成气体、沉淀、弱电解质、络合物或发生氧化还原反应、复分解反应的就能共存,据此分析解答.
解答:
解:A.Ca2+、SO42-反应生成微溶物硫酸钙,所以不能大量共存,故A错误;
B.这几种离子之间不反应,所以能大量共存,故B正确;
C.Fe2+、H+、SO32-、ClO-发生氧化还原反应生成硫酸根离子、铁离子和氯离子,所以不能大量共存,故C错误;
D.Fe3+、SCN-反应生成络合物硫氰化铁,所以不能大量共存,故D错误;
故选B.
B.这几种离子之间不反应,所以能大量共存,故B正确;
C.Fe2+、H+、SO32-、ClO-发生氧化还原反应生成硫酸根离子、铁离子和氯离子,所以不能大量共存,故C错误;
D.Fe3+、SCN-反应生成络合物硫氰化铁,所以不能大量共存,故D错误;
故选B.
点评:本题考查离子共存,为高考高频点,明确离子性质及离子共存条件即可解答,涉及氧化还原反应、络合反应、复分解反应,易错选项是C,注意酸性条件下,次氯酸根离子具有强氧化性,题目难度中等.

练习册系列答案
相关题目
某同学实际配制的NaOH溶液的浓度偏低,其原因不正确的是( )
| A、使用滤纸称量NaOH固体 |
| B、容量瓶中原来存在少量蒸馏水 |
| C、溶解后的烧杯未经洗涤 |
| D、定容时仰视刻度线 |
根据陈述的知识,类推得出的结论正确的是( )
| A、镁条在空气中燃烧生成的氧化物是MgO,则钠在空气中燃烧生成的氧化物是Na2O |
| B、已知ⅣA沸点CH4<SiH4<GeH4,则ⅤA族沸点 NH3<PH3<AsH3 |
| C、已知Fe与S直接化合生成FeS,则Cu与S直接化合生成Cu2S |
| D、已知Ca(HCO3)2+2NaOH(过量)=CaCO3↓+Na2CO3+2H2O,则Mg(HCO3)2+2NaOH(过量)=MgCO3↓+Na2CO3+2H2O |
下列说法正确的是( )
| A、从海水提取物质都必须通过化学反应才能实现 |
| B、“地沟油”经过加工处理后,可以用来制肥皂和生物柴油 |
| C、“绿色化学”的核心是利用化学原理进行环境治理 |
| D、生石灰、铁粉、硅胶是食品包装中常用的干燥剂 |
生活中下列物质的应用或现象解释错误的是( )
| A、食盐可作调味剂,也可作食品防腐剂 |
| B、大量燃烧化石燃料是造成雾霾天气的重要因素之一 |
| C、装饰材料释放的甲醛会造成空气污染 |
| D、磨豆浆的大豆富含蛋白质,豆浆煮沸后蛋白质变成了氨基酸 |
下列物质的水溶液能够导电,但属于非电解质的是( )
| A、四氯化碳 | B、二氧化硫 |
| C、氯化氢 | D、氯气 |
设NA为阿伏伽德罗常数的值.下列说法正确的是( )
A、5NH4NO3
| ||||
| B、室温下,1 L pH=13的NaOH溶液中,由水电离的OH-数目为0.1NA | ||||
| C、氢氧燃料电池正极消耗22.4 L(标准状况)气体时,电路中通过的电子数目为2NA | ||||
| D、高温下,0.2 mol Fe与足量水蒸气反应,生成的H2分子数目为0.3 NA |
 国务院总理温家宝在哥本哈根世界气候峰会上表示,中国正处于工业化、城镇化快速发展的关键阶段,能源结构以煤为主,降低排放存在特殊困难,但仍始终把应对气候变化作为重要战略任务.现在“低碳循环”已经引起了国民的重视,试回答下列问题:
国务院总理温家宝在哥本哈根世界气候峰会上表示,中国正处于工业化、城镇化快速发展的关键阶段,能源结构以煤为主,降低排放存在特殊困难,但仍始终把应对气候变化作为重要战略任务.现在“低碳循环”已经引起了国民的重视,试回答下列问题: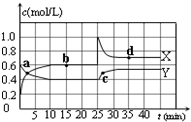 已知:2NO2(g)?N2O4(g);△H<0.在恒温恒容条件下,将一定量NO2和N2O4的混合气体通入容积为2L的密闭容器中,反应过程中各物质的物质的量浓度c随时间t的变化关系如图所示.
已知:2NO2(g)?N2O4(g);△H<0.在恒温恒容条件下,将一定量NO2和N2O4的混合气体通入容积为2L的密闭容器中,反应过程中各物质的物质的量浓度c随时间t的变化关系如图所示.