题目内容
8.有A、B、C、D四种元素,已知A元素原子的第一层和第三层电子数相同;B元素原子的第二层比第一层电子数多5个;C元素的+3价阳离子和氖原子具有相同的电子数;D元素的原子核外有4个电子层,第一层与第二层电子数之和等于第三层与第四层电子数之和.写出:(1)元素符号:AMg,BF,CAl,DCa.
(2)A、D的原子结构示意图
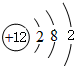 、
、 ,C的离子结构示意图
,C的离子结构示意图
(3)化合物AB2的电子式
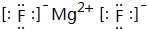 化学键类型为离子键.
化学键类型为离子键.
分析 A、B、C、D四种元素,A元素原子的第一层和第三层电子数相同,第三层电子数为2,故A为Mg;B元素原子的第二层比第一层电子数多5个,第二层电子数为7,故B为F元素;C元素的+3价阳离子和氖原子具有相同的电子数,则C为Al;D元素的原子核外有4个电子层,第一层与第二层电子数之和等于第三层与第四层电子数之和,则第三层、第四层电子数之和为10,说明原子核外各层电子数分别为2、8、8、2,故D为Ca元素,据此解答.
解答 解:(1)A、B、C、D四种元素,A元素原子的第一层和第三层电子数相同,第三层电子数为2,故A为Mg;B元素原子的第二层比第一层电子数多5个,第二层电子数为7,故B为F元素;C元素的+3价阳离子和氖原子具有相同的电子数,则C为Al;D元素的原子核外有4个电子层,第一层与第二层电子数之和等于第三层与第四层电子数之和,则第三层、第四层电子数之和为10,说明原子核外各层电子数分别为2、8、8、2,故D为Ca元素,
故答案为:Mg;F;Al;Ca;
(2)A为Mg,原子结构示意图为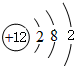 ,D为Ca,原子结构示意图为
,D为Ca,原子结构示意图为 ,C的离子为Al3+,离子结构示意图为
,C的离子为Al3+,离子结构示意图为 ,
,
故答案为: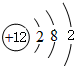 ;
; ;
; ;
;
(3)A与B所形成的化合物为MgF2,电子式为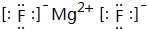 ,含有离子键,
,含有离子键,
故答案为: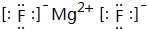 ,离子键.
,离子键.
点评 本题考查结构与位置关系应用,关键是理解掌握核外电子排布规律,侧重对化学用语的考查,难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
9.用石墨电极电解含有一定量重水(D2O)的水(H2O),下列说法正确的是( )
| A. | 两电极上产生的气体质量之比为4:1 | |
| B. | 两电极上产生的气体质量之比为8:1 | |
| C. | 相同状况下两电极上产生的气体体积之比为1:1 | |
| D. | 若两电极上产生的气体质量比为16:3,则D2O与H2O的物质的量之比为1:1 |
10.工业上常用氧化黄铁矿的方法制备硫酸亚铁:2FeS2+7O2+2H2O=2FeSO4+2H2SO4,下列说法正确的是( )
| A. | FeS2既是氧化剂,又是还原剂 | |
| B. | FeSO4溶液保存过程中需加稀硫酸和铁粉,防止变质 | |
| C. | 每生产1molFeSO4,转移的电子数为28NA | |
| D. | 硫酸工业中煅烧黄铁矿,其氧化产物只有SO2 |
13.已知反应:①2C(s)+O2(g)=2CO(g)△H=-221kJ/mol
②稀溶液中,H+(aq)+OH-(aq)=H2O(l)△H=-57.3kJ/mol
下列结论正确的是( )
②稀溶液中,H+(aq)+OH-(aq)=H2O(l)△H=-57.3kJ/mol
下列结论正确的是( )
| A. | 碳的燃烧热为△H=-110.5 kJ/mol | |
| B. | 1molC(s)所具有的能量一定高于1molCO(g)所具有的能量 | |
| C. | 稀硫酸与稀NaOH溶液反应的中和热为△H=-57.3 kJ/mol | |
| D. | 稀醋酸与稀NaOH溶液反应生成1 mol水,也放出57.3 kJ 热量 |
17.下列原子或原子团不属于官能团的是( )
| A. | -CH3 | B. | -F | C. | -OH | D. | 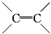 |
18.碳、氮广泛的分布在自然界中,碳、氮的化合物性能优良,在工业生产和科技领域有重要用途.
(1)氮化硅(Si3N4)是一种新型陶瓷材料,它可由SiO2与过量焦炭在1300~1700°C的氮气流中反应制得:3SiO2(s)+6C(s)+2N2(g)?Si3N4(s)+6CO(g)该反应放出1591.2kJ的能量,则该反应每转移1mole-,可放出的热量为132.6kJ.
(2)某研究小组现将三组CO(g)与H2O(g)的混合气体分别通入体积为2L的恒容密闭容器中,一定条件下发生反应:CO(g)+H2O(g)?CO2(g)+H2(g),得到如下数据:
①实验Ⅰ中,前5min的反应速率v(H2O)=0.15mol•L-1•min-1.
②下列能判断实验Ⅱ已经达到平衡状态的是be.
a.混合气体的密度保持不变 b.容器内CO、H2O、CO2、H2的浓度比不再变化
c.容器内压强不再变化 d.容器中气体的平均相对分子质量不随时间而变化
e. v正(CO)=v逆(H2 O)
③若实验Ⅲ的容器是绝热的密闭容器,实验测得H2O(g)的转化率H2O%随时间变化的示意图如图1所示,b点v正>v逆(填“<”、“=”或“>”).
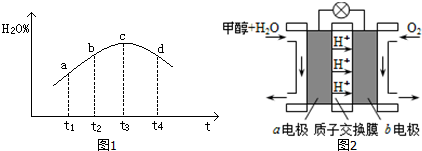
(3)利用CO与H2可直接合成甲醇,下图是由“甲醇(CH3OH)-空气”形成的绿色燃料电池的工作原理示意图2,写出以石墨为电极的电池工作时负极的电极反应式CH3OH-6e-+H2O=CO2+6H+.
(1)氮化硅(Si3N4)是一种新型陶瓷材料,它可由SiO2与过量焦炭在1300~1700°C的氮气流中反应制得:3SiO2(s)+6C(s)+2N2(g)?Si3N4(s)+6CO(g)该反应放出1591.2kJ的能量,则该反应每转移1mole-,可放出的热量为132.6kJ.
(2)某研究小组现将三组CO(g)与H2O(g)的混合气体分别通入体积为2L的恒容密闭容器中,一定条件下发生反应:CO(g)+H2O(g)?CO2(g)+H2(g),得到如下数据:
| 实验组 | 温度/℃ | 起始量/mol | 平衡量/mol | 达平衡所需时间/min | ||
| CO | H2O | CO | H2 | |||
| 1 | 650 | 2 | 4 | 0.5 | 1.5 | 5 |
| 2 | 900 | 1 | 2 | 0.5 | 0.5 | - |
②下列能判断实验Ⅱ已经达到平衡状态的是be.
a.混合气体的密度保持不变 b.容器内CO、H2O、CO2、H2的浓度比不再变化
c.容器内压强不再变化 d.容器中气体的平均相对分子质量不随时间而变化
e. v正(CO)=v逆(H2 O)
③若实验Ⅲ的容器是绝热的密闭容器,实验测得H2O(g)的转化率H2O%随时间变化的示意图如图1所示,b点v正>v逆(填“<”、“=”或“>”).

(3)利用CO与H2可直接合成甲醇,下图是由“甲醇(CH3OH)-空气”形成的绿色燃料电池的工作原理示意图2,写出以石墨为电极的电池工作时负极的电极反应式CH3OH-6e-+H2O=CO2+6H+.

 ;
;