题目内容
碱式碳酸铜的成分有多种,其化学式一般可表示为xCu(OH)2?yCuCO3.孔雀石呈绿色,是一种名贵的宝石,其主要成分是Cu(OH)2?CuCO3.某兴趣小组为探究制取孔雀石的最佳反应条件,设计了如下实验:
实验1:将2.0mL 0.50mol/LCu(NO3)2溶液、2.0mL 0.50mol/LNaOH溶液和0.25mol/L
Na2CO3溶液按表Ⅰ所示体积混合.
实验2:将合适比例的混合物在表Ⅱ所示温度下反应.
实验记录如下:
表Ⅰ表Ⅱ
(1)实验室制取少许孔雀石,应该采用的最佳反应条件:①Cu(NO3)2溶液与Na2CO3溶液的体积比为 ;②反应温度是 .
(2)80℃时,所制得的孔雀石有少量褐色物质的原因是 .
实验小组为测定上述某条件下所制得的碱式碳酸铜样品组成,利用下图所示的装置(夹持仪器省略)进行实验:
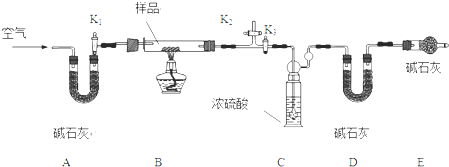
步骤1:检查装置的气密性,将过滤、洗涤并干燥过的样品置于平直玻璃管中.
步骤2:打开活塞K1、K2,关闭K3,鼓入空气,一段时间后关闭活塞K1、K2,打开K3,称量相关装置的质量.
步骤3:加热装置B直至装置C中无气泡产生.
(3)步骤4: .
步骤5:称量相关装置的质量.
(4)装置A的作用是 ;若无装置E,则实验测定的x/y的比值将 (选填“偏大”、“偏小”或“无影响”).
(5)某同学在实验过程中采集了如下数据:
a.反应前玻璃管与样品的质量163.8g
b.反应后玻璃管中残留固体质量56.0g
c.装置C实验后增重9.0g
d.装置D实验后增重8.8g
为测定
的比值,你认为可以选用上述所采集数据中的 (写出所有组合的字母代号)一组即可进行计算.
(6)根据你的计算结果,写出该样品组成的化学式 .
实验1:将2.0mL 0.50mol/LCu(NO3)2溶液、2.0mL 0.50mol/LNaOH溶液和0.25mol/L
Na2CO3溶液按表Ⅰ所示体积混合.
实验2:将合适比例的混合物在表Ⅱ所示温度下反应.
实验记录如下:
表Ⅰ表Ⅱ
| 编号 | V (Na2CO3)/mL | 沉淀情况 | 编号 | 反应温度/℃ | 沉淀情况 | |
| 1 | 2.8 | 多、蓝色 | 1 | 40 | 多、蓝色 | |
| 2 | 2.4 | 多、蓝色 | 2 | 60 | 少、浅绿色 | |
| 3 | 2.0 | 较多、绿色 | 3 | 75 | 较多、绿色 | |
| 4 | 1.6 | 较少、绿色 | 4 | 80 | 较多、绿色(少量褐色) |
(2)80℃时,所制得的孔雀石有少量褐色物质的原因是
实验小组为测定上述某条件下所制得的碱式碳酸铜样品组成,利用下图所示的装置(夹持仪器省略)进行实验:

步骤1:检查装置的气密性,将过滤、洗涤并干燥过的样品置于平直玻璃管中.
步骤2:打开活塞K1、K2,关闭K3,鼓入空气,一段时间后关闭活塞K1、K2,打开K3,称量相关装置的质量.
步骤3:加热装置B直至装置C中无气泡产生.
(3)步骤4:
步骤5:称量相关装置的质量.
(4)装置A的作用是
(5)某同学在实验过程中采集了如下数据:
a.反应前玻璃管与样品的质量163.8g
b.反应后玻璃管中残留固体质量56.0g
c.装置C实验后增重9.0g
d.装置D实验后增重8.8g
为测定
| x |
| y |
(6)根据你的计算结果,写出该样品组成的化学式
考点:探究物质的组成或测量物质的含量
专题:实验探究和数据处理题
分析:(1)根据表中碳酸钠溶液的体积与硝酸铜溶液的体积关系及最佳生成碱式碳酸铜温度完成,由表中数据,0.25mol?L-1的碳酸钠溶液2mL时生成的碱式碳酸铜最多,已知0.50mol/L Cu(NO3)2溶液为2.0mL,所以此时V[Cu(NO3)2]:V(Na2CO3)=1:1;
(2)所制得的孔雀石有少量褐色物质是氧化铜,氢氧化铜分解生成了黑色的氧化铜;
(3)依据实验步骤和目的分析,步骤4是反应完毕后,需要继续通空气,让装置冷却;
(4)根据实验目的和碱石灰的作用分析,装置A碱石灰是干燥剂,可吸收空气中的水分,同时还能吸收空气中的二氧化碳,防止对装置CD增重的数据造成影响,装置E的作用是防止空气中的二氧化碳和水蒸气进入D装置;
(5)根据化学方程式找出与x、y有关的物质质量,对比分析,碱式碳酸铜分解的化学方程xCu(OH)2?yCuCO3
(x+y)CuO+xH2O+yCO2↑要测定
的值,可以测定生成的水和二氧化碳的质量,即测定C装置增重的质量和D装置增重的质量或bc、bd装置质量计算判断.
(6)根据计算结果写出该样品组成的化学式.
(2)所制得的孔雀石有少量褐色物质是氧化铜,氢氧化铜分解生成了黑色的氧化铜;
(3)依据实验步骤和目的分析,步骤4是反应完毕后,需要继续通空气,让装置冷却;
(4)根据实验目的和碱石灰的作用分析,装置A碱石灰是干燥剂,可吸收空气中的水分,同时还能吸收空气中的二氧化碳,防止对装置CD增重的数据造成影响,装置E的作用是防止空气中的二氧化碳和水蒸气进入D装置;
(5)根据化学方程式找出与x、y有关的物质质量,对比分析,碱式碳酸铜分解的化学方程xCu(OH)2?yCuCO3
| ||
| x |
| y |
(6)根据计算结果写出该样品组成的化学式.
解答:
解:(1)由表中数据,0.25mol?L-1的碳酸钠溶液2mL时生成的碱式碳酸铜最多,已知0.50mol/L Cu(NO3)2溶液为2.0mL,所以此时V[Cu(NO3)2]:V(Na2CO3)=1:1;当温度在75℃,生成的碱式碳酸铜最佳,
故答案为:1:1;75℃;
(2)温度较高,氢氧化铜分解生成了氧化铜,所制得的孔雀石有少量褐色物质是氧化铜;
故答案为:Cu(OH)2受热分解为CuO;
(3)步骤4反应完毕后,需要继续通空气,让装置冷却,
故答案为:打开K1,继续通一段时间空气至装置冷却;
(4)装置A碱石灰是干燥剂,可吸收空气中的水分,同时还能吸收空气中的二氧化碳,防止对装置CD增重的数据造成影响,装置E的作用是防止空气中的二氧化碳和水蒸气进入D装置,D装置是吸收生成的二氧化碳的,C装置是吸收生成的水的,如果没有装置E,会使D装置质量增重偏大,即生成的二氧化碳质量偏大,则
的值会偏小
故答案为:除去空气中的CO2和H2O; 偏小;
(5)碱式碳酸铜分解的化学方程xCu(OH)2?yCuCO3
(x+y)CuO+xH2O+yCO2↑要测定
的值,可以测定生成的水和二氧化碳的质量,即测定C装置增重的质量和D装置增重的质量.故可选cd,
xCu(OH)2?yCuCO3
(x+y)CuO+xH2O+yCO2↑
18x 44y
9g 8.8g
=
,所以
=
,
若测出反应后玻璃管中样品的质量以及装置C增重的质量,即已知方程式中氧化铜和水的质量关系,可求出
的值;故可选bc
xCu(OH)2?yCuCO3
(x+y)CuO+xH2O+yCO2↑
(x+y)×80 18x
56g 9g
=
,所以
=
同样若已知反应后玻璃管中样品的质量以及装置C增重的质量,即已知方程式中氧化铜和二氧化碳的质量关系,可求出
的值.故可可选bd;
xCu(OH)2?yCuCO3
(x+y)CuO+xH2O+yCO2↑
(x+y)×80 44y
56g 8.8
=
,所以
=
;
故答案为:bc、bd、cd;
(6)根据计算结果写出该样品组成的化学式:5Cu(OH)2?2CuCO3;
故答案为:5Cu(OH)2?2CuCO3.
故答案为:1:1;75℃;
(2)温度较高,氢氧化铜分解生成了氧化铜,所制得的孔雀石有少量褐色物质是氧化铜;
故答案为:Cu(OH)2受热分解为CuO;
(3)步骤4反应完毕后,需要继续通空气,让装置冷却,
故答案为:打开K1,继续通一段时间空气至装置冷却;
(4)装置A碱石灰是干燥剂,可吸收空气中的水分,同时还能吸收空气中的二氧化碳,防止对装置CD增重的数据造成影响,装置E的作用是防止空气中的二氧化碳和水蒸气进入D装置,D装置是吸收生成的二氧化碳的,C装置是吸收生成的水的,如果没有装置E,会使D装置质量增重偏大,即生成的二氧化碳质量偏大,则
| x |
| y |
故答案为:除去空气中的CO2和H2O; 偏小;
(5)碱式碳酸铜分解的化学方程xCu(OH)2?yCuCO3
| ||
| x |
| y |
xCu(OH)2?yCuCO3
| ||
18x 44y
9g 8.8g
| 18x |
| 9g |
| 44x |
| 8.8g |
| x |
| y |
| 5 |
| 2 |
若测出反应后玻璃管中样品的质量以及装置C增重的质量,即已知方程式中氧化铜和水的质量关系,可求出
| x |
| y |
xCu(OH)2?yCuCO3
| ||
(x+y)×80 18x
56g 9g
| (x+y)×80 |
| 56 |
| 18x |
| 9 |
| x |
| y |
| 5 |
| 2 |
同样若已知反应后玻璃管中样品的质量以及装置C增重的质量,即已知方程式中氧化铜和二氧化碳的质量关系,可求出
| x |
| y |
xCu(OH)2?yCuCO3
| ||
(x+y)×80 44y
56g 8.8
| (x+y)×80 |
| 56 |
| 44y |
| 8.8g |
| x |
| y |
| 5 |
| 2 |
故答案为:bc、bd、cd;
(6)根据计算结果写出该样品组成的化学式:5Cu(OH)2?2CuCO3;
故答案为:5Cu(OH)2?2CuCO3.
点评:本题考碱式碳酸铜样品组成,涉及了根据化学方程式计算分析物质组成,浓硫酸增重的质量是生成的水的质量,碱石灰增重的质量是生成的二氧化碳的质量.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
设NA表示阿伏加德罗常数,下列说法不正确的是( )
| A、甲烷的摩尔质量与NA个甲烷分子的质量在数值上相等 |
| B、NA个氧气分子和NA个氢气分子的质量比等于16:1 |
| C、28 g氮气所含的原子数目为NA |
| D、17克NH3所含的原子数目为4NA,所含电子数目为10NA |
 某溶液中可能含有OH-,CO32-,AlO2-,SiO32-,SO42-,K+,Na+,Fe3+,Mg2+,Al3+等离子,当向溶液中逐滴加入一定物质的量的盐酸时,生成沉淀物质的量与加入盐酸体积的关系如图所示.下列判断正确的是( )
某溶液中可能含有OH-,CO32-,AlO2-,SiO32-,SO42-,K+,Na+,Fe3+,Mg2+,Al3+等离子,当向溶液中逐滴加入一定物质的量的盐酸时,生成沉淀物质的量与加入盐酸体积的关系如图所示.下列判断正确的是( )| A、原溶液中一定含有Na2SO4 |
| B、反应后形成的溶液溶质为NaCl |
| C、原溶液中含有CO32-与AlO2-的物质的量比为3:4 |
| D、原溶液中一定含有的离子是OH-,CO32-,SiO32-,AlO2-,K+ |
根据等电子原理,下列分子或离子与SO42-有相似结构的是( )
| A、PCl5 |
| B、CCl4 |
| C、NF3 |
| D、N |

 能源是人类生存和发展的重要支柱,碳元素的单质及化合物是人类生产生活的主要能源物质.
能源是人类生存和发展的重要支柱,碳元素的单质及化合物是人类生产生活的主要能源物质.
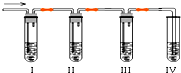 化学课外兴趣小组学生在实验室里制取的乙烯中常混有少量的二氧化硫,老师启发他们并由他们自己设计了下列实验图以确认上述混合气体中有C2H4和SO2.回答下列问题:
化学课外兴趣小组学生在实验室里制取的乙烯中常混有少量的二氧化硫,老师启发他们并由他们自己设计了下列实验图以确认上述混合气体中有C2H4和SO2.回答下列问题: