题目内容
11.在盛有水的电解槽中加入含等物质的量的Ag+,Pb2+,K+,SO 2-,NO-,Br- 的物质,充分搅拌,然后用惰性电极电解,通电片刻后,氧化产物和还原产物的物质的量之比为( )| A. | 1:2 | B. | 8:1 | C. | 1:1 | D. | 800:108 |
分析 在盛有水的电解槽中加入含等物质的量的Ag+,Pb2+,K+,SO42-,NO3-,Br-的物质,充分搅拌,发生的离子反应Ag++Br-=AgBr↓、Pb2++SO42-=PbSO4 ↓,所以溶液中溶质为KNO3,用惰性电极电解该溶液,阳极上氢氧根离子放电,阴极上氢离子放电,则氧化产物是氧气,还原产物是氢气.
解答 解:在盛有水的电解槽中加入含等物质的量的Ag+,Pb2+,K+,SO42-,NO3-,Br-的物质,充分搅拌,发生的离子反应Ag++Br-=AgBr↓、Pb2++SO42-=PbSO4 ↓,所以溶液中溶质为KNO3,用惰性电极电解该溶液,阳极上氢氧根离子放电,阴极上氢离子放电,则氧化产物是氧气,还原产物是氢气,依据化学方程式2H2O$\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑知,氧化产物和还原产物的物质的量之比为1:2,
故选A.
点评 本题考查电解原理和离子共存,为高频考点,正确判断溶液中溶质成分是解本题关键,侧重考查学生分析判断能力,学生在解答过程中易漏掉离子共存而导致错误,为易错题.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
1.一定浓度的醋酸溶液,在下列溶剂中电离程度最大的是( )
| A. | H2O | B. | 液NH3 | C. | 液态HF | D. | 纯H2SO4 |
2.设NA代表阿伏伽德罗常数的值,下列叙述正确的是( )
| A. | 常温下,100 mL 1 mol•L-1 Na2CO3溶液中含有的阴离子数大于0.1NA | |
| B. | 常温常压下,28g14CO和N2的混合物所含的质子数为14NA | |
| C. | 将NA个NH3分子溶于1L水中得到1 mol•L-1的氨水 | |
| D. | 1molCl2分别与足量的铁或氢氧化钠溶液反应,转移电子数均为2NA |
19.O2F2 可以发生反应:H2S+4O2F2═SF6+2HF+4O2,下列说法正确的是( )
| A. | 氧气是氧化产物 | |
| B. | O2F2是氧化剂 | |
| C. | 若生成 4.48 L HF,则转移 0.8 mol 电子 | |
| D. | 还原剂与氧化剂的物质的量之比为 4:1 |
6.下列物质性质与应用对应关系正确的是( )
| A. | 次氯酸有酸性,可用于漂白、杀菌消毒 | |
| B. | 纯碱能与酸反应,可用作治疗胃酸过多的药物 | |
| C. | 液氨汽化时要吸收大量的热,工业上可用作制冷剂 | |
| D. | 晶体硅的熔点高、硬度大,可用于制作半导体材料 |
16.化学与社会、生活密切相关.下列现象或事实以及解释均正确的是( )
| 选项 | 现象或事实 | 解释 |
| A | 在入海口的钢铁闸门上装一定数量的锌块可防止闸门被腐蚀 | 钢铁闸门与锌块在海水中构成原电池,钢铁闸门作正极 |
| B | 某些抗氧化剂作食品添加剂 | 抗氧化剂与食品反应,延缓食品腐败速率 |
| C | 用热的烧碱溶液洗去油污 | Na2CO3可直接与油污反应 |
| D | 明矾可作漂白剂 | 明矾电离出的Al3+水解时产生具有吸附性的胶体粒子 |
| A. | A | B. | B | C. | C | D. | D |
3.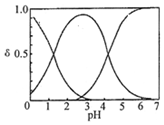 H2C2O4水溶液中H2C2O4、HC2O4-和C2O42-三种形态的粒子的分布分数δ随溶液pH变化的关系如图所示[已知Ksp(CaC2O4)=2.3×10-9].下列说法正确的是( )
H2C2O4水溶液中H2C2O4、HC2O4-和C2O42-三种形态的粒子的分布分数δ随溶液pH变化的关系如图所示[已知Ksp(CaC2O4)=2.3×10-9].下列说法正确的是( )
 H2C2O4水溶液中H2C2O4、HC2O4-和C2O42-三种形态的粒子的分布分数δ随溶液pH变化的关系如图所示[已知Ksp(CaC2O4)=2.3×10-9].下列说法正确的是( )
H2C2O4水溶液中H2C2O4、HC2O4-和C2O42-三种形态的粒子的分布分数δ随溶液pH变化的关系如图所示[已知Ksp(CaC2O4)=2.3×10-9].下列说法正确的是( )| A. | 0.1mol•L-1H2C2O4溶液使KMnO4溶液褪色的离子方程式:2MnO4-+5C2O42-+16H+═2Mn2++10CO2↑+8H2O | |
| B. | 0.1 mol•L-1 NaHC2O4溶液中:c(C2O42-)>c(H2C2O4) | |
| C. | pH=5时,溶液中主要含碳微粒浓度大小关系为:c(C2O42-)>c(H2C2O4)>c(HC2O4-) | |
| D. | 一定温度下,往CaC2O4饱和溶液中加入少量CaCl2固体,c(C2O42-)将减小,c(Ca2+)不变 |
20.下列物质露置于空气中易变质的是( )
①氯水 ②水玻璃 ③烧碱 ④漂白粉 ⑤绿矾 ⑥亚硫酸钠 ⑦浓硫酸 ⑧浓硝酸.
①氯水 ②水玻璃 ③烧碱 ④漂白粉 ⑤绿矾 ⑥亚硫酸钠 ⑦浓硫酸 ⑧浓硝酸.
| A. | 除⑤外 | B. | 除②③外 | C. | 除②③⑥外 | D. | 均易变质 |
20.X、Y、Z、M、W为五种短周期元素.X、Y、Z是原子序数依次递增的同周期元素,且最外层电子数之和为15,X与Z可形成XZ2分子;Y与M形成的气态化合物在标准状况下的密度为0.76g•L-1;W的质子数是X、Y、Z、M四种元素质子数之和的$\frac{1}{2}$.下列说法正确的是( )
| A. | 原子半径:W>Z>Y>X>M | |
| B. | XZ2、X2M2、W2Z2均为直线型的共价化合物 | |
| C. | 由X元素形成的单质可能导电 | |
| D. | 由X、Y、Z、M四种元素形成的化合物一定既有离子键,又有共价键 |