题目内容
11.100mL 6mol•L-1H2SO4跟过量锌粉反应,一定温度下,为了减缓反应进行的速率,但又不影响生成氢气的总量,可向反应物中加入适量( )| A. | 碳酸钠(固体) | B. | 少量硫酸铜溶液 | C. | Na2SO4溶液 | D. | 加热 |
分析 根据反应的实质为Zn+2H+═Zn2++H2↑,为了减缓反应速率,但又不影响生成氢气的总量,则减小氢离子的浓度但不能改变氢离子的物质的量即可,注意Zn过量,以此来解答.
解答 解:A.碳酸钠与酸反应,生成氢气的量减少,故A错误;
B.锌置换出铜,形成铜锌原电池,反应速率增大,故B错误;
C.加适量的Na2SO4溶液,相当于稀释,氢离子的物质的量不变,浓度变小,则减缓反应进行的速率,但又不影响生成氢气的总量,故C正确;
D.热溶液温度升高,反应速率增大,故D错误.
故选C.
点评 本题考查影响化学反应速率的因素,为高频考点,明确浓度对反应速率的影响即可解答,选项B为学生解答中的难点,注意原电池反应的特点,题目难度不大.

练习册系列答案
相关题目
1.烯烃在一定条件下发生氧化反应时C=C键发生断裂,如RCH=CHR’,可以氧化成RCHO和R’CHO,在该条件下,下列烯烃分别被氧化后产物可能有乙醛的是( )
| A. | CH3CH=CH(CH2)2CH3 | B. | CH2=CH(CH2)2CH3 | ||
| C. | CH3CH2 CH=CH2 | D. | CH3CH2CH=CHCH2CH3 |
19.X和Y元素的原子,在化学反应中都容易失去电子而形成与Ne相同的电子层结构,已知X的原子序数比Y的原子序数大,下列说法中正确的是( )
| A. | X的金属性比Y的金属性强 | |
| B. | 常温下,X和Y都不能从水中置换出氢 | |
| C. | Y元素的氢氧化物碱性比X 元素的氢氧化物碱性弱 | |
| D. | X元素的最高化合价比Y 元素的最高化合价高 |
6.设NA表示阿伏加德罗常数的值.下列说法不正确的是( )
| A. | 标准状况下,2.24 L甲醛中含氧原子数目为0.1NA | |
| B. | 常温下,28g C2H4含NA个碳碳双键 | |
| C. | 常温常压下,1 mol羟基所含的电子数为9NA | |
| D. | 常温常压下,10 g 46%酒精水溶液中含氧原子总数为0.1NA |
3.以下对生活事实的解释,不正确的是( )
| A. | 厨房里洗涤油污,常用碱性洗涤剂,因为植物油会在碱性溶液中水解 | |
| B. | 用灼烧的方法可以区别人造丝和蚕丝,因为蚕丝是蛋白质,被灼热时会产生具有烧焦羽毛的气味 | |
| C. | 食品添加剂虽然能改善食物的色、香、味,但由于他们对健康有害,均不宜食用 | |
| D. | 高温消毒是通过加热的方法使细菌的蛋白质变性而死亡 |
20.下列化学用语正确的是( )
| A. | H2S的电子式: | B. | Mg2+的结构示意图: | ||
| C. | Na2O的电子式: | D. | N2的电子式: |
1.下列说法中正确的是( )
| A. | 铁是黑色金属,所以断口是黑色的 | B. | 铁是第ⅧB族元素,也是过渡元素 | ||
| C. | 在自然界中无游离态的铁存在 | D. | 自然界里含铁的矿物质叫铁矿石 |

 ,E
,E .
.

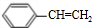 $\stackrel{催化剂}{→}$
$\stackrel{催化剂}{→}$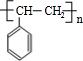 .
. 为了验证铜与稀硝酸反应产生的是一氧化氮而不是氢气.某校学生实验小组设计了一个实验,其装置如图所示(加热装置和固定装置均已略去).B为一个用金属丝固定的干燥管,内装块状碳酸钙固体;C中有足量的澄清石灰水,E为一个空的蒸馏烧瓶;F是用于鼓入空气的双连打气球.
为了验证铜与稀硝酸反应产生的是一氧化氮而不是氢气.某校学生实验小组设计了一个实验,其装置如图所示(加热装置和固定装置均已略去).B为一个用金属丝固定的干燥管,内装块状碳酸钙固体;C中有足量的澄清石灰水,E为一个空的蒸馏烧瓶;F是用于鼓入空气的双连打气球.