题目内容
2.已知同周期非金属元素X、Y的非金属性:X>Y,下列说法错误的是( )| A. | X的原子序数一定大于Y | B. | 第一电离能Y可能大于X | ||
| C. | 简单离子的半径:Xm->Yn- | D. | 气态氢化物的稳定性:HmX强于HnY |
分析 同周期元素,自左而右元素的非金属性增强,非金属性:X>Y,故原子序数X>Y,电负性大的元素的第一电离能不一定大,同周期从左到右阴离子的半径减小,结合元素周期律分析.
解答 解:同周期元素,自左而右元素的非金属性增强,非金属性:X>Y,故原子序数X>Y.
A.由分析可知,原子序数X>Y,故A正确;
B.若Y的第一电离能失去的电子所处能级为半满稳定状态,其第一电离能可能高于X的第一电离能,如第一电离能P>S,故B正确;
C.同周期从左到右原子序数越大阴离子的半径越小,则简单离子的半径:Xm-<Yn-,故C错误;
D.非金属性越强,最高价含氧酸的酸性越强,同周期自左而右元素的非金属性增强,故非金属性X>Y,所以氢化物的稳定性:HmX强于HnY,故D正确;
故选C.
点评 本题考查同周期元素性质递变规律、电离能、电负性等,题目难度不大,注意同周期元素中第一电离能异常情况,侧重于考查学生的分析能力.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
14.下列有关实验的操作正确的是( )
| A. | 检验某补铁药片(主要成分为亚铁化合物)是否氧化变质,使用氯水和硫氰化钾溶液 | |
| B. | 测定溶液pH时,可用pH试纸蘸取少量待测液,并与标准比色卡比较 | |
| C. | 容量瓶、量筒和滴定管上都标有使用温度,量筒、容量瓶无“0”刻度,滴定管有“0”刻度,使用时滴定管水洗后还需润洗,但容量瓶水洗后不用润洗 | |
| D. | 测定碳酸钠中碳酸氢钠的含量:取a克样品与足量稀盐酸充分反应,逸出的气体通过碱石灰后,碱石灰增重b克,根据a和b的值即可求得碳酸氢钠的含量 |
13.下列各项中的离子方程式,书写正确的是( )
| A. | H2S?2H++S2- | |
| B. | NaHCO3电离:NaHCO3?Na++HCO3- | |
| C. | 一水合氨电离:NH3•H2O═NH4++OH- | |
| D. | 过量的CO2气体通入饱和石灰水中:CO2+OH-═HCO3- |
7.电解质量分数为5.2%的NaOH溶液1L(密度为1.06g/cm3),用铂作电极电解,当溶液中NaOH的质量分数改变了1.0% 时停止电解,此时溶液中符合下表关系的是( )
| NaOH的质量分数 | 阳极析出物质的质量/g | 阴极析出物质的质量/g | |
| A | 6.2% | 19 | 152 |
| B | 6.2% | 152 | 19 |
| C | 4.2% | 1.2 | 9.4 |
| D | 4.2% | 9.4 | 1.2 |
| A. | A | B. | B | C. | C | D. | D |
14.已知某种微生物燃料电池工作原理如图所示.下列有关该电池的说法中,正确的是( )
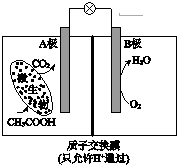

| A. | 外电路电子从B极移向A极 | |
| B. | 溶液中H+由B极区移向A极区 | |
| C. | 电池工作一段时间后B极区溶液的pH减小 | |
| D. | A极电极反应式为:CH3COOH-8e-+2H2O=2CO2+8H+ |
11.化学与科学、技术、军事密切相关.下列说法正确的是( )
| A. | 光导纤维遇强碱会“断路” | |
| B. | 苹果放在空气中久置变黄和纸张久置变黄原理相似 | |
| C. | “辽宁舰”上用于舰载机降落拦阻索的特种钢缆,属于新型无机非金属材料 | |
| D. | “歼-20”飞机上使用的碳纤维是一种新型的有机高分子材料 |
12.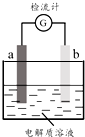 30℃时,利用图装置进行实验,结果记录如下表所示:
30℃时,利用图装置进行实验,结果记录如下表所示:
下列说法不正确的是( )
 30℃时,利用图装置进行实验,结果记录如下表所示:
30℃时,利用图装置进行实验,结果记录如下表所示:| 实验 | a电极 | b电极 | 电解质溶液 | 现象 |
| I | Cu | Zn | 稀H2SO4 | 检流计指针向左偏转 |
| Ⅱ | Fe | Al | 稀H2SO4 | 检流计指针向左偏转 |
| Ⅲ | Fe | Al | 浓H2SO4 | 检流计指针先向左偏转,后逐渐归零,a电极表面逐渐变黑,b电极表面逐渐变白 |
| Ⅳ | Fe | Al | 浓HNO3 | 检流计指针迅速向右偏转,a电极逐渐溶解,b电极表面逐渐变白 |
| A. | Ⅱ中Al为负极,其电极反应是:Al-3e-═Al3+ | |
| B. | Ⅱ中的现象说明Fe和Al表面形成致密的氧化膜,阻止了电极反应的进行 | |
| C. | Ⅳ中Fe为负极,发生了氧化反应 | |
| D. | 上述实验表明:相同条件下,Fe在浓HNO3中更稳定,Al在浓H2SO4中更稳定 |