题目内容
氯碱工业的产物NaOH与不同物质反应可以生成不同的盐.已知常温下,浓度均为0.1mol/L的4种钠盐溶液pH如下表:下列说法中,正确的是( )
| 溶质 | Na2CO3 | NaHCO3 | NaClO | NaHSO3 |
| pH | 11.6 | 9.7 | 10.3 | 5.2 |
| A、常温下,相同物质的量浓度的H2SO3、H2CO3、HClO,pH最大的是H2SO3 |
| B、四种溶液中,水的电离程度最大的是NaClO |
| C、向氯水中加入少量NaHCO3可以增大氯水中次氯酸的浓度 |
| D、NaHSO3溶液中离子浓度大小顺序为:c(Na+)>c(H+)>c(HSO3-)>c(SO32-)>c(OH-) |
考点:盐类水解的应用,离子浓度大小的比较
专题:盐类的水解专题
分析:根据相同浓度的钠盐溶液pH大小知,酸根离子水解程度大小顺序是:CO32->ClO->HCO3->HSO3-,则酸的强弱顺序是H2SO3>H2CO3>HClO>HCO3-,
A.酸根离子水解程度越大,则酸的酸性越弱;
B.相同浓度的这几种钠盐溶液中,溶液pH越大则水的电离程度越大;
C.盐酸和碳酸氢钠反应生成氯化钠和二氧化碳,促进氯气和水反应;
D.亚硫酸氢钠溶液呈酸性,说明HSO3-电离程度大于水解程度,无论电离还是水解其程度都较小.
A.酸根离子水解程度越大,则酸的酸性越弱;
B.相同浓度的这几种钠盐溶液中,溶液pH越大则水的电离程度越大;
C.盐酸和碳酸氢钠反应生成氯化钠和二氧化碳,促进氯气和水反应;
D.亚硫酸氢钠溶液呈酸性,说明HSO3-电离程度大于水解程度,无论电离还是水解其程度都较小.
解答:
解:根据相同浓度的钠盐溶液pH大小知,酸根离子水解程度大小顺序是:CO32->ClO->HCO3->HSO3-,则酸的强弱顺序是H2SO3>H2CO3>HClO>HCO3-,
A.酸根离子水解程度越大,则酸的酸性越弱,酸根离子水解程度大小顺序是:CO32->ClO->HCO3->HSO3-,则酸的强弱顺序是H2SO3>H2CO3>HClO>HCO3-,所以常温下,相同物质的量浓度的H2SO3、H2CO3、HClO溶液,HClO的酸性最弱,所以pH最大的是HClO溶液,故A错误;
B.相同浓度的这几种钠盐溶液中,溶液pH越大则水的电离程度越大,根据表中数据知,水的电离程度最大的是碳酸钠溶液,故B错误;
C.盐酸和碳酸氢钠反应生成氯化钠和二氧化碳,促进氯气和水反应,次氯酸和碳酸氢钠不反应,所以导致溶液中次氯酸浓度增大,故C正确;
D.亚硫酸氢钠溶液呈酸性,说明HSO3-电离程度大于水解程度,无论电离还是水解其程度都较小,所以c(H+)<c(HSO3-),
则离子浓度大小顺序为:c(Na+)>c(HSO3-)>c(H+)>c(SO32-)>c(OH-),故D错误;
故选C.
A.酸根离子水解程度越大,则酸的酸性越弱,酸根离子水解程度大小顺序是:CO32->ClO->HCO3->HSO3-,则酸的强弱顺序是H2SO3>H2CO3>HClO>HCO3-,所以常温下,相同物质的量浓度的H2SO3、H2CO3、HClO溶液,HClO的酸性最弱,所以pH最大的是HClO溶液,故A错误;
B.相同浓度的这几种钠盐溶液中,溶液pH越大则水的电离程度越大,根据表中数据知,水的电离程度最大的是碳酸钠溶液,故B错误;
C.盐酸和碳酸氢钠反应生成氯化钠和二氧化碳,促进氯气和水反应,次氯酸和碳酸氢钠不反应,所以导致溶液中次氯酸浓度增大,故C正确;
D.亚硫酸氢钠溶液呈酸性,说明HSO3-电离程度大于水解程度,无论电离还是水解其程度都较小,所以c(H+)<c(HSO3-),
则离子浓度大小顺序为:c(Na+)>c(HSO3-)>c(H+)>c(SO32-)>c(OH-),故D错误;
故选C.
点评:本题考查了盐类水解,根据钠盐溶液pH大小确定相对应酸的强弱,再结合强酸制取弱酸、酸式酸根离子电离和水解程度相对大小等知识点来分析解答,题目难度中等.

练习册系列答案
 名师指导期末冲刺卷系列答案
名师指导期末冲刺卷系列答案 开心蛙口算题卡系列答案
开心蛙口算题卡系列答案
相关题目
对于苯乙烯 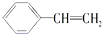 的下列叙述:①能使酸性KMnO4溶液褪色,②可发生加聚反应,③可溶于水,④可溶于苯中,⑤苯环能与溴水发生取代反应,⑥所有的原子可能共面.其中完全正确的是( )
的下列叙述:①能使酸性KMnO4溶液褪色,②可发生加聚反应,③可溶于水,④可溶于苯中,⑤苯环能与溴水发生取代反应,⑥所有的原子可能共面.其中完全正确的是( )
 的下列叙述:①能使酸性KMnO4溶液褪色,②可发生加聚反应,③可溶于水,④可溶于苯中,⑤苯环能与溴水发生取代反应,⑥所有的原子可能共面.其中完全正确的是( )
的下列叙述:①能使酸性KMnO4溶液褪色,②可发生加聚反应,③可溶于水,④可溶于苯中,⑤苯环能与溴水发生取代反应,⑥所有的原子可能共面.其中完全正确的是( )| A、①②④ | B、①②④⑥ |
| C、①②④⑤⑥ | D、①②③④⑤⑥ |
已知某化学反应的平衡常数表达式为K=
,在不同的温度下该反应的平衡常数如下表:下列有关叙述不正确的是( )
| cCO2?cH2 |
| cCO?cH2O |
| t/℃ | 700 | 800 | 830 | 1000 | 1200 |
| K | 1.67 | 1.11 | 1.00 | 0.60 | 0.38 |
| A、若在1 L的密闭容器中通入CO2和H2各1 mol,5 min后温度升高到830℃,此时测得CO2为0.4 mol时,该反应达到平衡状态 | ||||
| B、上述反应的正反应是放热反应 | ||||
| C、该反应的化学方程式是CO(g)+H2O(g)?CO2(g)+H2(g) | ||||
D、若平衡浓度符合下列关系式:
|
某研究小组对离子方程式xR2++yH++O2=mR3++nH2O的分析研究,下列说法中错误的是( )
| A、根据电荷守恒,得出x与y的和一定等于m |
| B、根据原子守恒,得出x和m的数值一定相等 |
| C、根据电子得失守恒,得出x=4的结论 |
| D、根据氧化还原反应关系得出:R2+是还原剂,O2是氧化剂,R3+是氧化产物,H2O是还原产物 |
下列各种应用中,利用了硅元素的还原性的是( )
| A、用硅制造集成电路、晶体管等半导体器件 | ||||
| B、在野外,用硅、石灰、烧碱的混合物制取氢气:Si+Ca (OH)2+2NaOH=Na2SiO3+CaO+2H2↑ | ||||
| C、用HF酸刻蚀玻璃:SiO2+4HF=SiF4↑+2H2O | ||||
D、单质硅的制备:SiO2+2C
|

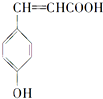 咖啡酸具有止血功效,存在于多种中药中,其结构简式为
咖啡酸具有止血功效,存在于多种中药中,其结构简式为