题目内容
10.往AgNO3、Cu(NO3)2、Zn(NO3)2的混合溶液中加入一些铁粉,待反应完成后过滤,可能存在的情况是( )| A. | 滤纸上有Ag,滤液中有Ag+、Cu2+、Zn2+、Fe2+ | |
| B. | 滤纸上有Ag、Cu,滤液中有Ag+、Zn2+、Fe2+ | |
| C. | 滤纸上有Ag、Cu、Fe,滤液中有Cu2+、Zn2+、Fe2+ | |
| D. | 纸上有Ag、Cu、Fe、Zn,滤液中有Zn2+ |
分析 根据金属活动顺序表可知金属的活泼性:锌>铁>铜>银,铁不能与硝酸锌反应,故滤液中一定含有Zn2+,铁能与硝酸铜反应生成硝酸亚铁和铜,能与硝酸银反应生成硝酸亚铁和银,故滤液只一定含有Fe2+,铜能与硝酸银反应生成硝酸铜和银,故滤纸上一定含有银,据此进行解答.
解答 解:在金属活动性顺序中,锌>铁>铜>银,铁不能与硝酸锌反应,故滤液中一定含有Zn2+,铁能与硝酸铜反应生成硝酸亚铁和铜,能与硝酸银反应生成硝酸亚铁和银,故滤液只一定含有Fe2+,铜能与硝酸银反应生成硝酸铜和银,故滤纸上一定含有银,
A.若加入的铁粉量少,只能与部分硝酸银反应生成银,故滤纸上有Ag,滤液中有Ag+、Cu2+、Zn2+、Fe2+,故A正确;
B.当滤纸上含有Ag和Cu,则滤液中不能含有Ag+,因为铜能将银离子置换为银,故B错误;
C.当铁加入过量时,能将全部的硝酸银和硝酸铜置换出来,铁粉有剩余,则滤纸上有Ag、Cu、Fe,滤液中有Zn2+、Fe2+,不可能含有Cu2+,故C错误;
D.铁不能与硝酸锌反应,故滤纸上不含有锌,故D错误;
故选A.
点评 本题考查了金属活动性顺序的应用,题目难度不大,明确常见金属的活泼性强弱为解答关键,中置换的先后顺序为:活动性最弱的金属置换出来,然后依活动性由弱到强依次置换,试题培养了学生的分析能力及灵活应用能力.

练习册系列答案
相关题目
18.下列图象所表示的化学知识中,不正确的是( )
| A. | 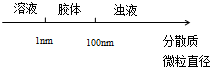 分散系的分类 | B. | 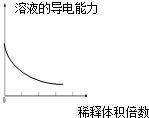 稀释浓氢氧化钠溶液的过程 | ||
| C. | 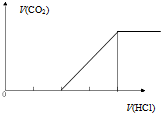 向碳酸钠溶液中逐滴滴加盐酸 | D. |  向偏铝酸钠溶液中逐滴滴加盐酸 |
15.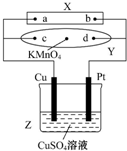 图中X为电源,Y为浸透饱和食盐水和酚酞试液的滤纸,滤纸中央滴有一滴KMnO4溶液,通电后Y中央的紫红色斑向d端扩散.下列判断正确的是( )
图中X为电源,Y为浸透饱和食盐水和酚酞试液的滤纸,滤纸中央滴有一滴KMnO4溶液,通电后Y中央的紫红色斑向d端扩散.下列判断正确的是( )
 图中X为电源,Y为浸透饱和食盐水和酚酞试液的滤纸,滤纸中央滴有一滴KMnO4溶液,通电后Y中央的紫红色斑向d端扩散.下列判断正确的是( )
图中X为电源,Y为浸透饱和食盐水和酚酞试液的滤纸,滤纸中央滴有一滴KMnO4溶液,通电后Y中央的紫红色斑向d端扩散.下列判断正确的是( )| A. | 滤纸上c点附近会变红色 | B. | Cu电极质量减小,Pt电极质量增大 | ||
| C. | Z中溶液的pH先减小,后增大 | D. | 溶液中的SO42-向Cu电极定向移动 |
2.下列叙述正确的是( )
①非金属元素构成的物质的化学键都是共价键
②两种不同非金属元素原子间形成的化学键都是极性键
③金属元素构成的化合物里一定含有离子键
④难失去电子的原子,易形成阴离子
⑤单质分子中不存在化学键,化合物的分子才存在化学键
⑥离子化合物中一定含有离子键.
①非金属元素构成的物质的化学键都是共价键
②两种不同非金属元素原子间形成的化学键都是极性键
③金属元素构成的化合物里一定含有离子键
④难失去电子的原子,易形成阴离子
⑤单质分子中不存在化学键,化合物的分子才存在化学键
⑥离子化合物中一定含有离子键.
| A. | 只有②⑥ | B. | 只有①⑤⑥ | C. | 只有③⑥ | D. | 只有①④⑥ |
20.化合物 与NaOH溶液、碘水三者混和后可发生如下反应:
与NaOH溶液、碘水三者混和后可发生如下反应:
①I2+2NaOH=NaI+NaIO+H2O
②
③
此反应称为碘仿反应,根据上述反应方程式推断下列物质中能发生碘仿反应的有( )
 与NaOH溶液、碘水三者混和后可发生如下反应:
与NaOH溶液、碘水三者混和后可发生如下反应:①I2+2NaOH=NaI+NaIO+H2O
②

③

此反应称为碘仿反应,根据上述反应方程式推断下列物质中能发生碘仿反应的有( )
| A. | CH3CHO | B. | CH3CH2CHO | ||
| C. | CH3CH2COCH2CH3 | D. | CH3CH2COCH2 CH2CH3 |
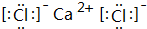 .
.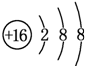 ;D与E能形成一种结构类似于CO2的三原子分子,且每个原子均达到了8电子的稳定结构,该分子的结构式为S=C=S.
;D与E能形成一种结构类似于CO2的三原子分子,且每个原子均达到了8电子的稳定结构,该分子的结构式为S=C=S.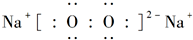 (填电子式),其化学键类型为离子键、非极性共价键(填“离子键”、“非极性共价键”、“极性共价键”中的一种或多种).
(填电子式),其化学键类型为离子键、非极性共价键(填“离子键”、“非极性共价键”、“极性共价键”中的一种或多种).