题目内容
2.下列叙述正确的是( )①非金属元素构成的物质的化学键都是共价键
②两种不同非金属元素原子间形成的化学键都是极性键
③金属元素构成的化合物里一定含有离子键
④难失去电子的原子,易形成阴离子
⑤单质分子中不存在化学键,化合物的分子才存在化学键
⑥离子化合物中一定含有离子键.
| A. | 只有②⑥ | B. | 只有①⑤⑥ | C. | 只有③⑥ | D. | 只有①④⑥ |
分析 ①非金属元素可以形成离子键;
②两种不同非金属元素原子吸引电子能力不同;
③金属元素构成的化合物不一定含有离子键;
④稀有气体元素的原子不容易得失电子;
⑤双原子或多原子分子中存在化学键;
⑥含有离子键的化合物是离子化合物.
解答 解:①非金属元素可以形成离子键,如氯化铵是离子化合物,由非金属元素构成,故错误;
②两种不同非金属元素原子吸引电子能力不同,形成的共用电子对会偏向吸引电子能力强的一方,使分子有极性,形成极性键,故正确;
③金属元素构成的化合物不一定含有离子键,如氯化铝是含有金属元素的共价化合物,不含有离子键,故错误;
④难失去电子的原子,不一定易形成阴离子,如稀有气体元素的原子不容易得失电子,故错误;
⑤双原子或多原子分子中存在化学键,如氯气中含有Cl-Cl键,错误;
⑥依据共价化合物和离子化合物的概念可知共价化合物中只有共价键,离子化合物中一定有离子键,含有离子键的化合物是离子化合物,故错误;
故选A.
点评 本题考查了化学键和化合物的关系,明确离子键、共价键、离子化合物、共价化合物的内涵是解题的关键,难度不大.

练习册系列答案
 黄冈创优卷系列答案
黄冈创优卷系列答案
相关题目
12.下列有关元素周期表的说法错误的是( )
| A. | 可在金属与非金属交界处寻找半导体材料 | |
| B. | 农药中常含有的元素通常在元素周期表的右上方区域内 | |
| C. | 作催化剂材料的元素通常在元素周期表的左下方区域内 | |
| D. | 在过渡元素中可寻找耐高温和耐腐蚀的合金材料 |
10.往AgNO3、Cu(NO3)2、Zn(NO3)2的混合溶液中加入一些铁粉,待反应完成后过滤,可能存在的情况是( )
| A. | 滤纸上有Ag,滤液中有Ag+、Cu2+、Zn2+、Fe2+ | |
| B. | 滤纸上有Ag、Cu,滤液中有Ag+、Zn2+、Fe2+ | |
| C. | 滤纸上有Ag、Cu、Fe,滤液中有Cu2+、Zn2+、Fe2+ | |
| D. | 纸上有Ag、Cu、Fe、Zn,滤液中有Zn2+ |
7.下列各组元素性质的递变情况正确的是( )
| A. | Na、Mg、Al原子最外层电子数依次增多 | |
| B. | P、S、Cl元素最高正价依次降低 | |
| C. | N、O、F原子半径依次增大 | |
| D. | Na、K、Rb的金属性依次减弱 |
14.下列热化学方程式中,△H能正确表示物质的燃烧热的是( )
| A. | 2CO(g)+O2(g)═2CO2(g)△H=-566.0 kJ/mol | |
| B. | C(s)+$\frac{1}{2}$O2(g)═CO(g)△H=-110.5 kJ/mol | |
| C. | CH4(g)+2O2(g)═CO2(g)+2H2O(l)△H=-890.31 kJ/mol | |
| D. | 2C8H18(l)+25O2(g)═16CO2(g)+18H2O(l)△H=-11036 kJ/mol |
11.有八种物质:①甲烷、②苯、③聚乙烯、④2-戊烯、⑤2-丁炔、⑥甲苯、⑦苯乙烯,⑧聚氯乙烯.其中既能使酸性高锰酸钾溶液褪色,又能使溴水因化学反应而褪色的是( )
| A. | ③④⑤⑧ | B. | ④⑤⑦ | C. | ④⑤ | D. | ③④⑤⑦⑧ |
12.非金属性最强的元素是( )
| A. | C | B. | F | C. | S | D. | Cl |
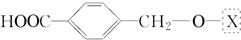 ,为了研究X的结构,将化合物A在一定条件下水解只得到B(分子式为C8H8O3)和C(分子式为C7H6O3).C遇FeCl3水溶液显紫色,与NaHCO3溶液反应有CO2产生.
,为了研究X的结构,将化合物A在一定条件下水解只得到B(分子式为C8H8O3)和C(分子式为C7H6O3).C遇FeCl3水溶液显紫色,与NaHCO3溶液反应有CO2产生.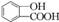 .
. 任意2种.
任意2种.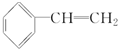 为主要原料制备
为主要原料制备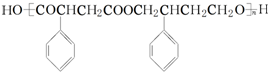 的合成路线流程图(无机试剂任选).
的合成路线流程图(无机试剂任选).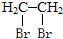
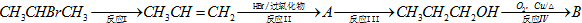 请回答下列问题:
请回答下列问题: