题目内容
10.下列物质性质与用途的对应关系不正确的是( )| 选项 | 性质 | 用途 |
| A | 氧化铁呈红棕色 | 红色涂料 |
| B | 氧化铝熔点很高 | 耐火材料 |
| C | 浓硫酸具有脱水性 | 干燥剂 |
| D | 液氨汽化时要吸收大量的热 | 制冷剂 |
| A. | A | B. | B | C. | C | D. | D |
分析 A、氧化铁是红棕色固体;
B、氧化铝熔点很高,耐火灼烧;
C、浓硫酸做干燥剂是由于其能吸水;
D、液氨汽化时吸热,会导致周围温度降低.
解答 解:A、氧化铁是红棕色固体,可以作红色涂料,故A正确;
B、氧化铝熔点很高,在较高温度下不熔化,故可以做耐火材料,故B正确;
C、浓硫酸做干燥剂是由于其能吸水,有吸水性,而非脱水性,故C错误;
D、液氨汽化时吸热,会导致周围温度降低,故可以做制冷剂,故D正确.
故选C.
点评 本题考查了物质的物理性质和其用途之间的关系,难度不大,把握住“性质决定用途,用途反映性质”这一条线.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
20.甲醇是一种重要的化工原料,广泛应用于化工生产,也可以直接用作燃料.
已知:CH3OH(l)+O2(g)=CO(g)+2H2O(g)△H=-443.64kJ•mol-1
2CO(g)+O2(g)=2CO2(g)△H2=-566.0kJ•mol-1
下列说法或热化学方程式正确的是( )
已知:CH3OH(l)+O2(g)=CO(g)+2H2O(g)△H=-443.64kJ•mol-1
2CO(g)+O2(g)=2CO2(g)△H2=-566.0kJ•mol-1
下列说法或热化学方程式正确的是( )
| A. | CO的燃烧热为566.0 kJ•mol-1 | |
| B. | 2 mol CO和1 mol O2的总能量比2 mol CO2的总能量低 | |
| C. | 完全燃烧20g甲醇,生成二氧化碳和液态水时放出的热量为908.3 kJ | |
| D. | 2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(g)a=-1453.28 kJ•mol-1 |
18.下列同周期元素中,原子半径最小的是( )
| A. | Mg | B. | Al | C. | Si | D. | S |
5.下列有关物质性质的比较,不正确的是( )
| A. | 金属性:Al>Mg | B. | 稳定性:HF>HCl | ||
| C. | 酸性:HClO4>H2SO4 | D. | 碱性:NaOH>Mg(OH)2 |
19.如表实验能达到预期目的是( )
| 实验内容 | 实验目的 | |
| A | 向新制氯水中滴加少量紫色石蕊试液,充分振荡后溶液先变红色后褪色 | 证明有氯水具有酸性 |
| B | 将Cl2通入NaBr溶液中,溶液变黄 | 比较氯气比液溴的氧化性强 |
| C | 向FeCl3和CuCl2混合溶液中加入铁粉,有红色固体析出 | 证明氧化性:Cu2+>Fe3+ |
| D | 向某待测溶液中,加入BaCl2溶液,产生白色沉淀,继续滴加稀盐酸,沉淀不消失 | 证明待测溶液中含有SO42- |
| A. | A | B. | B | C. | C | D. | D |
20.某次实验室制取乙酸丁酯所用原料为:7.4mL1-丁醇、6.0mL冰醋酸,1.0mL浓硫酸.若制得乙酸丁酯(式量116)的质量为5.12g,则以下正确的是( )
| 1-丁醇 | 冰醋酸 | |
| 密度(g/cm3) | 0.81 | 1.05 |
| 摩尔质量(g/mol) | 74 | 60 |
| A. | 产率:约54.49% | B. | 产率:约42.04% | ||
| C. | 转化率:冰醋酸小于1-丁醇 | D. | 转化率:冰醋酸大于1-丁醇 |

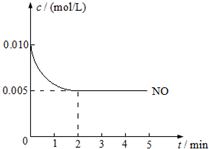 2NO(g)+O2(g)?2NO2(g)△H<0是制造硝酸的重要反应之一.在800℃时,向容积为1L的密闭容器中充入0.010mol NO和0.005molO2,反应过程中NO的浓度随时间变化如图所示:
2NO(g)+O2(g)?2NO2(g)△H<0是制造硝酸的重要反应之一.在800℃时,向容积为1L的密闭容器中充入0.010mol NO和0.005molO2,反应过程中NO的浓度随时间变化如图所示: