题目内容
一定条件下,向含HNO3的废水中加入CH3OH进行污水处理,发生反应5CH3OH+6HNO3=3N2↑+5CO2↑+13H2O,下列说法正确的是( )
| A、CH3OH被氧化,表现氧化性 |
| B、此条件下还原性强弱为:N2>CH3OH |
| C、若氧化产物比还原产物多0.2mol,则该反应中转移3mol |
| D、该反应过程中断裂的化学键既有极性键又有非极性键 |
考点:氧化还原反应
专题:
分析:A.CH3OH被氧化,表现还原性;
B.还原剂的还原性大于还原产物的还原性;
C.反应中每生成3molN2转移30mol电子,结合方程式计算;
D.CH3OH和HNO3中没有非极性键.
B.还原剂的还原性大于还原产物的还原性;
C.反应中每生成3molN2转移30mol电子,结合方程式计算;
D.CH3OH和HNO3中没有非极性键.
解答:
解:A.5CH3OH+6HNO3=3N2↑+5CO2↑+13H2O中N元素的化合价降低被还原,则HNO3作氧化剂,具有氧化性,CH3OH被氧化,表现还原性,故A错误;
B.还原剂的还原性大于还原产物的还原性,反应中CH3OH为还原剂,N2为还原产物,则此条件下还原性强弱为:CH3OH>N2,故B错误;
C.5CH3OH+6HNO3=3N2↑+5CO2↑+13H2O中每生成3molN2转移30mol电子,若氧化产物比还原产物多0.2mol,则还原产物N2的物质的量为0.3mol,所以则该反应中转移3mol,故C正确;
D.CH3OH和HNO3中没有非极性键,只含有极性键,则该反应过程中断裂的化学键只有极性键,故D错误.
故选C.
B.还原剂的还原性大于还原产物的还原性,反应中CH3OH为还原剂,N2为还原产物,则此条件下还原性强弱为:CH3OH>N2,故B错误;
C.5CH3OH+6HNO3=3N2↑+5CO2↑+13H2O中每生成3molN2转移30mol电子,若氧化产物比还原产物多0.2mol,则还原产物N2的物质的量为0.3mol,所以则该反应中转移3mol,故C正确;
D.CH3OH和HNO3中没有非极性键,只含有极性键,则该反应过程中断裂的化学键只有极性键,故D错误.
故选C.
点评:本题考查了氧化还原反应,难度不大,侧重于学生的分析能力和计算能力的考查,注意从元素化合价的角度解答该题.

练习册系列答案
 53随堂测系列答案
53随堂测系列答案
相关题目
如图所示是298K时,N2与H2反应过程中能量变化的曲线图,下列叙述正确的是( )
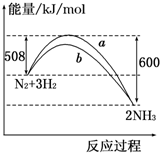

| A、该反应的热化学方程式为:N2+3H2?2NH3△H=-92 kJ/mol |
| B、a曲线是加入催化剂时的能量变化曲线 |
| C、加入催化剂,该化学反应的反应热改变 |
| D、在温度、体积一定的条件下,若通入2 mol N2和6 mol H2反应后放出的热量为Q kJ,则184>Q |
一定温度下,对于反应N2+O2?2NO在密闭容器中进行,下列措施一定能加快反应速率的是( )
| A、使压强增大 |
| B、恒容,充入N2 |
| C、恒容,充入He气 |
| D、恒压,充入He气 |
下列关于钠的说法不正确的是( )
| A、金属钠和氧气反应,条件不同,产物不同 |
| B、钠长期置于空气中,表面不能形成致密氧化膜 |
| C、钠与水反应时,钠熔成小球在水面四处游动 |
| D、由于钠比较活泼,所以它能从溶液中置换出金属活动性顺序表中钠后面的金属 |
 (1)金刚石和石墨均为碳的同素异形体,它们在氧气不足时燃烧生成一氧化碳,在氧气充足时充分燃烧生成二氧化碳,反应中放出的热量如图所示.
(1)金刚石和石墨均为碳的同素异形体,它们在氧气不足时燃烧生成一氧化碳,在氧气充足时充分燃烧生成二氧化碳,反应中放出的热量如图所示.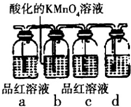 掌握物质之间的转化,是学习元素化合物知识的基础.
掌握物质之间的转化,是学习元素化合物知识的基础.