题目内容
20g烧碱配制成 500mL溶液,其物质的量浓度为 mol?L-1;从中取出1mL,其中含溶质为 g.若将这1mL溶液用水稀释到100mL,所得溶液中含Na+ g.
考点:物质的量浓度的相关计算
专题:
分析:根据n=
以及c=
计算溶液的物质的量浓度;
溶液为均一稳定分散系,取出任意体积都和原溶液浓度相等;
根据溶液稀释前后溶质的物质的量不变计算稀释后溶质的物质的量浓度.
| m |
| M |
| n |
| V |
溶液为均一稳定分散系,取出任意体积都和原溶液浓度相等;
根据溶液稀释前后溶质的物质的量不变计算稀释后溶质的物质的量浓度.
解答:
解:20g烧碱的物质的量为:n=
=0.5mol,则c=
=1mol/L;
溶液为均一稳定分散系,取出任意体积都和原溶液浓度相等,从中取出1mL,其物质的量浓度为1mol/L;
溶质的质量为:m=nM=cVM=0.001L×1mol/L×40g/mol=0.04g;
溶液稀释前后溶质的物质的量不变,这1mL溶液用水稀释到100mL,所得溶液中溶质的物质的量0.001L×1mol/L=0.001mol,所以含Na+的物质的量为0.001mol,质量为0.001mol×23g/mol=0.023g,
故答案为:1;0.04;0.023.
| 20g |
| 40g/mol |
| 0.5mol |
| 0.5L |
溶液为均一稳定分散系,取出任意体积都和原溶液浓度相等,从中取出1mL,其物质的量浓度为1mol/L;
溶质的质量为:m=nM=cVM=0.001L×1mol/L×40g/mol=0.04g;
溶液稀释前后溶质的物质的量不变,这1mL溶液用水稀释到100mL,所得溶液中溶质的物质的量0.001L×1mol/L=0.001mol,所以含Na+的物质的量为0.001mol,质量为0.001mol×23g/mol=0.023g,
故答案为:1;0.04;0.023.
点评:本题考查物质的量浓度计算,题目难度不大,注意有关计算公式的运用,把握溶液的特点以及溶液稀释前后溶质的物质的量不变的特征.

练习册系列答案
相关题目
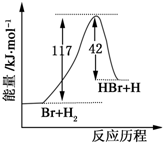
参照反应Br2+H2→HBr+H的能量随反应历程变化的示意图,下列叙述中正确的是( )

| A、反应物具有的总能量大于生成物具有的总能量 |
| B、正反应为吸热反应 |
| C、逆反应为吸热反应 |
| D、从图中可看出,该反应的反应热与反应途径有关 |
一定条件下,向含HNO3的废水中加入CH3OH进行污水处理,发生反应5CH3OH+6HNO3=3N2↑+5CO2↑+13H2O,下列说法正确的是( )
| A、CH3OH被氧化,表现氧化性 |
| B、此条件下还原性强弱为:N2>CH3OH |
| C、若氧化产物比还原产物多0.2mol,则该反应中转移3mol |
| D、该反应过程中断裂的化学键既有极性键又有非极性键 |
已知:A(g)+O2(g)═AO2(g)△H=-393.5kJ/mol;2B2(g)+O2(g)═2B2O(g)△H=-483.6kJ/mol.现有0.4mol的A和B2组成的混合气,在氧气中完全燃烧,共放出127.06kJ热量,则混合物中A与B2的物质的量之比为( )
| A、2:3 | B、1:2 |
| C、1:1 | D、3:2 |
若20g密度为ρ g?cm-3的硝酸钙溶液里含1g Ca2+,则NO3-的物质的量浓度是( )
A、
| ||
B、
| ||
| C、2.5ρ mol?L-1 | ||
| D、1.25ρ mol?L-1 |
M(NO3)2热分解化学方程式为:2M(NO3)2
2MO+4NO2↑+O2↑,加热37.6g M(NO3)2使其完全分解,在标准状况下收集11200mL的气体,那么M的摩尔质量是( )
| ||
| A、24g/mol |
| B、64g/mol |
| C、65g/mol |
| D、40g/mol |
下列反应的离子方程式错误的是( )
| A、向碳酸氢钙溶液中加入过量氢氧化钠 Ca2++2HCO3-+2OH-=CaCO3↓+2H2O+CO32- |
| B、氢氧化钡溶液与硫酸氢钠溶液1:1混合Ba2++OH-+H++SO42-=BaSO4↓+H2O |
| C、氢氧化钙溶液和碳酸氢镁反应:Ca2++OH-+HCO3-═CaCO3↓+H2O |
| D、向溴化亚铁溶液中通入过量氯气:2Fe2++4Br-+3Cl2═2Fe3++2Br2+6Cl- |