题目内容
6. 早在1807年化学家戴维用电解熔融氢氧化钠制得钠:4NaOH(熔)$\frac{\underline{\;电解\;}}{\;}$4Na+O2↑+2H2O;后来盖•吕萨克用铁与熔融氢氧化钠作用也制得钠:3Fe+4NaOH$\frac{\underline{\;1100℃\;}}{\;}$Fe3O4+2H2↑+4Na↑.下列有关说法正确的是( )
早在1807年化学家戴维用电解熔融氢氧化钠制得钠:4NaOH(熔)$\frac{\underline{\;电解\;}}{\;}$4Na+O2↑+2H2O;后来盖•吕萨克用铁与熔融氢氧化钠作用也制得钠:3Fe+4NaOH$\frac{\underline{\;1100℃\;}}{\;}$Fe3O4+2H2↑+4Na↑.下列有关说法正确的是( )| A. | 电解熔融氢氧化钠制钠,阳极发生电解反应2OH--2e-═H2↑+O2↑ | |
| B. | 盖•吕萨克法制钠原理是利用铁的还原性比钠强 | |
| C. | 若戴维法与盖•吕萨克法制得等量的钠,则两反应中转移的电子总数不同 | |
| D. | 目前工业上常用电解熔融氯化钠法制钠(如上图),电解槽中石墨极为阴极,铁为阳极 |
分析 A.阳极氢氧根离子放电生成氧气和水;
B.1100℃时生成Na蒸气,有利于反应正向移动;
C.戴维法生成4molNa转移4mol电子,但盖•吕萨克法生成4molNa转移8mol电子;
D.石墨极为阳极,氯离子放电,在阴极钠离子放电.
解答 解:A.由4NaOH(熔)$\frac{\underline{\;电解\;}}{\;}$4Na+O2↑+2H2O可知,阳极氢氧根离子放电生成氧气和水,电极反应为4OH--4e-=2H2O+O2↑,故A错误;
B.1100℃时生成Na蒸气,有利于反应正向移动,但Na的还原性大于Fe,故B错误;
C.由4NaOH(熔)$\frac{\underline{\;电解\;}}{\;}$4Na+O2↑+2H2O、3Fe+4NaOH$\frac{\underline{\;电解\;}}{\;}$Fe3O4+2H2↑十4Na↑可知,戴维法生成4molNa转移4mol电子,但盖•吕萨克法生成4molNa转移8mol电子,则转移电子不等,故C正确;
D.石墨极为阳极,氯离子放电,在阴极钠离子放电,发生2NaCl$\frac{\underline{\;电解\;}}{\;}$2Na+Cl2↑,故D错误;
故选D.
点评 本题考查金属的冶炼及电解原理,明确元素的化合价变化及发生的电极反应即可解答,题目难度不大,试题培养了学生的分析能力及灵活应用能力.

练习册系列答案
 英才计划期末调研系列答案
英才计划期末调研系列答案 精英口算卡系列答案
精英口算卡系列答案
相关题目
14.海水是巨大的资源宝库,海水中主要离子的含量如表所示.
从海水中提取食盐和溴的工艺流程如图:
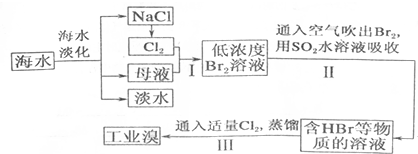
(1)请列举海水淡化的一种方法蒸留法或电渗透法或离子交换法等.
(2)请写出步骤I反应的离子方程式为Cl2+2Br-=Br2+2Cl-.
(3)步骤I中已经获得Br2,步骤II中又将获得的Br2还原为Br-,其目的是富集溴元素.
(4)步骤II用SO2水溶液吸收Br2,吸收率可达95%,该反应的离子方程式为SO2+Br2+2H2O═4H++2Br-+SO42-.
(5)依据上述流程,若将10m3海水中的溴元素转化为工业溴,至少需要标准状况下Cl2的体积为179.2L(忽略Cl2的溶解)
| 成分 | 含量(mg•L-1) | 成分 | 含量(mg•L-1) |
| Cl- | 18980 | Ca2+ | 400 |
| Na+ | 10560 | HCO3- | 142 |
| SO42- | 2560 | Br- | 64 |
| Mg2+ | 1272 |

(1)请列举海水淡化的一种方法蒸留法或电渗透法或离子交换法等.
(2)请写出步骤I反应的离子方程式为Cl2+2Br-=Br2+2Cl-.
(3)步骤I中已经获得Br2,步骤II中又将获得的Br2还原为Br-,其目的是富集溴元素.
(4)步骤II用SO2水溶液吸收Br2,吸收率可达95%,该反应的离子方程式为SO2+Br2+2H2O═4H++2Br-+SO42-.
(5)依据上述流程,若将10m3海水中的溴元素转化为工业溴,至少需要标准状况下Cl2的体积为179.2L(忽略Cl2的溶解)
11.世界上60%的镁是从海水中提取的,其主要步骤如下:
①把贝壳制成生石灰;
②在海水中加入生石灰,过滤、洗涤沉淀物;
③将沉淀物与盐酸反应,结晶、过滤;
④在氯化氢热气流中加热晶体;
⑤电解上述所得盐(熔融条件下).
下列说法正确的是( )
①把贝壳制成生石灰;
②在海水中加入生石灰,过滤、洗涤沉淀物;
③将沉淀物与盐酸反应,结晶、过滤;
④在氯化氢热气流中加热晶体;
⑤电解上述所得盐(熔融条件下).
下列说法正确的是( )
| A. | 向洗涤液中滴加氯化钙溶液可检验沉淀是否洗涤干净 | |
| B. | 上述变化过程中包括了分解、化合、复分解、置换等四种反应类型 | |
| C. | 步骤④在氯化氢热气流中加热晶体的目的是为了防止氯化镁水解 | |
| D. | 步骤⑤也可以采用电解该盐水溶液的方法 |
18.下列化合物中,含有离子键的是( )
| A. | CO2 | B. | HCl | C. | NH3 | D. | NaCl |
15.在15.2g铁和铜的合金中加入过量的硝酸溶液,合金完全溶解,同时生成气体X,再向所得溶液中加入足量的NaOH溶液,生成25.4g沉淀,则下列X的组成合理的是( )
| A. | 0.3molNO2、0.1molNO | B. | 0.6molNO | ||
| C. | 0.3molNO、0.1molNO2 | D. | 0.2molNO2、0.2molNO |
6.下列物质既能跟稀硫酸反应,又能跟氢氧化钠溶液反应的是( )
①Al2O3 ②Al(OH)3 ③Al.
①Al2O3 ②Al(OH)3 ③Al.
| A. | ①②③ | B. | ①和③ | C. | ②和③ | D. | ①和② |
 .
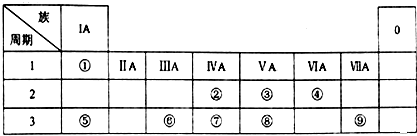
. ⑧的最高价氧化物的水化物的分子式H3PO4.
⑧的最高价氧化物的水化物的分子式H3PO4. .
.