题目内容
2.下列属于氧化还原反应的是( )| A. | MgCl2+Ba(OH)2═BaCl2+Mg(OH)2↓ | B. | CO2+2NaOH═Na2CO3+H2O | ||
| C. | CaCO3 $\frac{\underline{\;高温\;}}{\;}$CaO+CO2↑ | D. | H2+CuO $\frac{\underline{\;\;△\;\;}}{\;}$H2O+Cu |
分析 氧化还原反应的实质为电子转移、特征为化合价升降,所以氧化还原反应中一定存在元素化合价变化,据此对各选项进行判断.
解答 解:A.MgCl2+Ba(OH)2═BaCl2+Mg(OH)2↓,为复分解反应,不存在化合价变化,不属于氧化还原反应,故A错误;
B.CO2+2NaOH═Na2CO3+H2O,不存在化合价变化,不属于氧化还原反应,故B错误;
C.CaCO3$\frac{\underline{\;高温\;}}{\;}$CaO+CO2↑为分解反应,反应中不存在化合价变化,不属于氧化还原反应,故C错误;
D.H2+CuO $\frac{\underline{\;\;△\;\;}}{\;}$H2O+Cu为为置换反应,H、Cu元素的化合价发生变化,属于氧化还原反应,故D正确;
故选D.
点评 本题考查了氧化还原反应的判断,题目难度不大,明确氧化还原反应的实质、特征为解答关键,注意掌握四种基本反应类型与氧化还原反应之间的关系,试题有利于提高学生的灵活应用能力.

练习册系列答案
 快乐5加2金卷系列答案
快乐5加2金卷系列答案
相关题目
13.下列关于有机物的说法中,正确的是( )
| A. | 塑料、橡胶和纤维一定都是合成高分子材料 | |
| B. | 蔗糖不是高分子化合物,其水解产物能发生银镜反应 | |
| C. | 某烃类的混合气体跟Cl2混合光照,有油状液滴生成,说明混合气体肯定含有甲烷 | |
| D. |  分子中所有原子不可能都共平面. 分子中所有原子不可能都共平面. |
17.下列说法正确的是( )
| A. | 原子核外电子排布式为1s2的原子与原子核外电子排布式为1s22s2的原子化学性质相似 | |
| B. | Zn2+的最外层电子排布式为3s23p63d10 | |
| C. | 基态铜原子的外围电子排布图: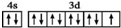 | |
| D. | 基态碳原子的最外层电子排布图: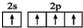 |
7.根据下列化学方程式:
①2MnO4-+16H++10Cl-═2Mn2++5Cl2↑+8H2O
②2Fe2++Cl2═2Fe3++2Cl-
③2Fe3++Cu═2Fe2++Cu2+
④Fe+Cu2+═Fe2++Cu
可判断MnO4-、Cu2+、Fe3+、Cl2的氧化性由强到弱的顺序为( )
①2MnO4-+16H++10Cl-═2Mn2++5Cl2↑+8H2O
②2Fe2++Cl2═2Fe3++2Cl-
③2Fe3++Cu═2Fe2++Cu2+
④Fe+Cu2+═Fe2++Cu
可判断MnO4-、Cu2+、Fe3+、Cl2的氧化性由强到弱的顺序为( )
| A. | Fe3+>MnO4->Cl2>Cu2+ | B. | MnO4->Cl2>Fe3+>Cu2+ | ||
| C. | Cl2>MnO4->Fe3+>Cu2+ | D. | Cu2+>Cl2>MnO4->Fe3+ |
12.下列几种说法中正确的是( )
| A. | 摩尔是化学上常用的一个物理量 | |
| B. | 某物质含有6.02×1023个微粒,含有这个数目微粒的物质一定是1 mol | |
| C. | 1摩尔氢气分子可以表示为1 mol H2 | |
| D. | 硫酸的摩尔质量为98 g |
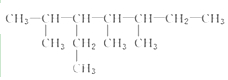 ;
;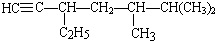 的系统名称为5,6-二甲基-3-乙基-1-庚烯,将其在催化剂存在条件下完全氢化,所得烷烃的系统名称为2,3-二甲基-5-乙基-庚烷.
的系统名称为5,6-二甲基-3-乙基-1-庚烯,将其在催化剂存在条件下完全氢化,所得烷烃的系统名称为2,3-二甲基-5-乙基-庚烷.