题目内容
 四种短周期元素A、B、C、D在元素周期表中的相对位置如图所示,其中D形成的两种氧化物都是大气污染物.下列有关判断正确的是( )
四种短周期元素A、B、C、D在元素周期表中的相对位置如图所示,其中D形成的两种氧化物都是大气污染物.下列有关判断正确的是( )| A、简单氢化物的热稳定性:C>A |
| B、最高价氧化物对应水化物的酸性:D<C |
| C、B的最高价氧化物的水化物能与D的最高价氧化物的水化物反应 |
| D、A、C、D的最高价含氧酸的钠盐水溶液可能均显碱性 |
考点:位置结构性质的相互关系应用
专题:元素周期律与元素周期表专题
分析:短周期元素D形成的两种氧化物都是大气污染物,D为S,根据相对位置可知A为C、B为Al、C为Si,
A、同一主族自上而下非金属性逐渐减弱,非金属性越强,气态氢化物越稳定;
B、同一周期从左到右非金属性逐渐增强,非金属性越强,最高价氧化物对应水化物的酸性越强;
C、氢氧化铝和硫酸能发生中和反应;
D、硫酸是强酸,硫酸钠溶液呈中性.
A、同一主族自上而下非金属性逐渐减弱,非金属性越强,气态氢化物越稳定;
B、同一周期从左到右非金属性逐渐增强,非金属性越强,最高价氧化物对应水化物的酸性越强;
C、氢氧化铝和硫酸能发生中和反应;
D、硫酸是强酸,硫酸钠溶液呈中性.
解答:
解:短周期元素D形成的两种氧化物都是大气污染物,D为S,根据相对位置可知A为C、B为Al、C为Si,
A、非金属性C>Si,气态氢化物的稳定性:CH4>SiH4,故A错误;
B、非金属性D>C,最高价氧化物对应水化物的酸性越强D>C,故B错误;
C、B的最高价氧化物的水化物是氢氧化铝,D的最高价氧化物的水化物是硫酸,氢氧化铝和硫酸能发生中和反应,故C正确;
D、硫酸是强酸,硫酸钠溶液呈中性,故D错误;
故选C.
A、非金属性C>Si,气态氢化物的稳定性:CH4>SiH4,故A错误;
B、非金属性D>C,最高价氧化物对应水化物的酸性越强D>C,故B错误;
C、B的最高价氧化物的水化物是氢氧化铝,D的最高价氧化物的水化物是硫酸,氢氧化铝和硫酸能发生中和反应,故C正确;
D、硫酸是强酸,硫酸钠溶液呈中性,故D错误;
故选C.
点评:本题主要是元素“位、构、性”三者关系的综合考查,比较全面考查学生有关元素推断知识,侧重于学生的分析能力的考查,为高考常见题型,难度中等,注意把握原子结构与元素周期律的递变规律.

练习册系列答案
相关题目
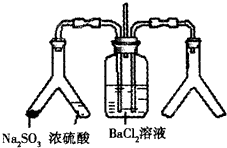 将SO2通入BaCl2溶液并不产生沉淀,而通入另一种气体后可以产生白色沉淀.则右侧Y形管中放置的药品组合不符合要求的是(必要时可以加热)( )
将SO2通入BaCl2溶液并不产生沉淀,而通入另一种气体后可以产生白色沉淀.则右侧Y形管中放置的药品组合不符合要求的是(必要时可以加热)( )| A、石灰石和稀硝酸 |
| B、CaO和氯化铵 |
| C、Cu和浓硝酸 |
| D、Na2O2和食盐水 |
现有1.0mol/L的NaOH溶液0.1L,若通入标准状况下体积为2.24L 的SO2气体,使其充分反应后,则所得溶液中各粒子浓度大小关系正确的是( )
| A、c(Na+)+c(H+)=c(HSO3-)+c(SO32-)+c( OH-) |
| B、c(Na+)=c(H2SO3)+c(HSO3-)+c( H+) |
| C、c(SO32-)+c( OH-)=c(H+)+c(H2SO3) |
| D、c(Na+)>c(HSO3-)>c( OH-)>c(H2SO3)>c(SO32-)>c(H+) |
用胆矾(化学式为CuSO4?5H2O,分子量为250)配制0.1mol/L的水溶液,下列方法正确的是( )
| A、取25 g CuSO4?5H2O溶于1 L水中 |
| B、将CuSO4?5H2O干燥去掉结晶水,取16g溶于水制成1 L溶液 |
| C、将25 g CuSO4?5H2O溶于水制成1 L溶液 |
| D、将16 gCuSO4?5H2O溶于水配成1 L溶液 |
在相同条件下,燃烧时对大气污染程度最小的燃料是( )
| A、液化气 | B、煤油 | C、煤球 | D、木柴 |
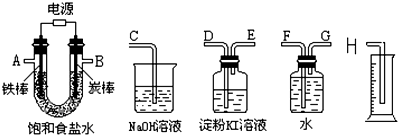
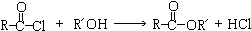
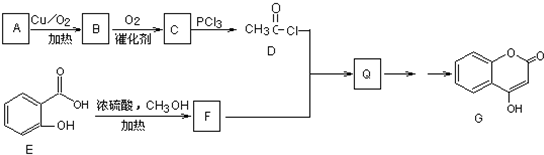
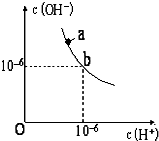 回答下列问题.
回答下列问题.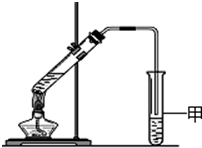 通过粮食发酵可获得某含氧有机物X,其相对分子质量为46,其中碳的质量分数为52.2%,氢的质量分数为13.0%.
通过粮食发酵可获得某含氧有机物X,其相对分子质量为46,其中碳的质量分数为52.2%,氢的质量分数为13.0%.