题目内容
15.某消毒液的主要成分为NaClO,还含有一定量的NaOH,下列叙述正确的是( )| A. | 用pH试纸测得该消毒液的pH约为12 | |
| B. | 该消毒液中,Fe3+、K+、NO${\;}_{3}^{-}$、CH3CHO可以大量共存 | |
| C. | 向该消毒液中滴入少量Na2SO3溶液,反应的离子方程为:SO${\;}_{3}^{2-}$+ClO-=Cl-+SO${\;}_{4}^{2-}$ | |
| D. | 向该消毒液中加入浓盐酸,每产生1mol Cl2,转移电子数约为2×6.02×1023 |
分析 A.NaClO具有漂白性,不能用pH试纸测定pH;
B.CH3CHO能被NaClO氧化;
C.NaClO与Na2SO3发生氧化还原反应生成NaCl和硫酸钠;
D.根据方程式ClO-+Cl-+2H+=Cl2↑+H2O计算.
解答 解:A.NaClO具有漂白性,能使pH褪色,所以不能用pH试纸测定pH,故A错误;
B.NaClO具有强氧化性,能与CH3CHO发生氧化还原反应,所以不能大量共存,故B错误;
C.NaClO与Na2SO3发生氧化还原反应生成NaCl和硫酸钠,其反应的离子方程式为:SO32-+ClO-=Cl-+SO42-,故C正确;
D.向该消毒液中加入浓盐酸,反应方程式为ClO-+Cl-+2H+=Cl2↑+H2O,反应中产生1mol Cl2转移电子1mol,即转移电子数约为6.02×1023,故D错误.
故选C.
点评 本题考查了氧化还原反应、离子共存、pH试纸的使用等,侧重于考查氧化还原反应以及物质氧化性的应用,题目难度中等,注意把握NaClO的性质.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
5.除去下列物质括号中的杂质,所采用方法不正确的是( )
| A. | 淀粉(氯化钠)渗析 | |
| B. | 硬脂酸钠(甘油溶液)盐析、过滤 | |
| C. | 水(鸡蛋清)蒸馏 | |
| D. | 蔗糖(葡萄糖)与银氨溶液混合水浴加热,过滤 |
6.下列排列顺序错误的是( )
| A. | 酸性:H4SiO4<H3PO4<H2SO4<HClO4 | B. | 碱性:Ca(OH)2>Mg(OH)2>Al(OH)3 | ||
| C. | 氢化物的稳定性:SiH4>H2S>H2O>HF | D. | 原子半径:F<O<S<Na |
3.由同一种元素所构成的不同单质被称为同素异形体,下列哪组物质不属于同素异形体的是( )
| A. | 钢和铁 | B. | 金刚石和石墨 | C. | 红磷和白磷 | D. | 氧气和臭氧 |
10.下表是有机物A、B的有关信息.
根据表中信息回答下列问题:
(1)A的名称为乙烯,A在一定条件下生成高分子化合物的反应方程式 .
.
(2)A与氢气发生加成反应后生成分子C,C在分子组成和结构上相似的有机物有一
大类(俗称“同系物”),它们均符合通式CnH2n+2.当n=4时,这类有机物开
始出现同分异构体.
(3)B具有的性质是②③(填序号).
①无色无味液体、②有毒、③不溶于水、④密度比水大、⑤与酸性KMnO4溶液和溴水
反应使之褪色、⑥任何条件下不与氢气反应.
(4)写出在浓硫酸作用下,B与浓硝酸反应的化学方程式:
 .
.
| A | B |
| ①能使溴的四氯化碳溶液褪色 ②比例模型为:  ③能与水在一定条件下反应生成醇 | ①由C、H两种元素组成 ②球棍模型为: 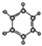 |
(1)A的名称为乙烯,A在一定条件下生成高分子化合物的反应方程式
 .
.(2)A与氢气发生加成反应后生成分子C,C在分子组成和结构上相似的有机物有一
大类(俗称“同系物”),它们均符合通式CnH2n+2.当n=4时,这类有机物开
始出现同分异构体.
(3)B具有的性质是②③(填序号).
①无色无味液体、②有毒、③不溶于水、④密度比水大、⑤与酸性KMnO4溶液和溴水
反应使之褪色、⑥任何条件下不与氢气反应.
(4)写出在浓硫酸作用下,B与浓硝酸反应的化学方程式:
 .
.
7.某可充电的锂离子电池以LiMn2O4为正极,嵌入锂的碳材料为负极,含Li+导电固体为电解质.放电时的电池反应为:Li+LiMn2O4═Li2Mn2O4.下列说法正确的是( )
| A. | 放电时,LiMn2O4发生氧化反应,电池内部Li+向正极移动 | |
| B. | 放电时,正极反应为:Li++LiMn2O4+e-═Li2Mn2O4 | |
| C. | 醋酸可用作锂离子电池的电解质 | |
| D. | 充电时,锂的碳材料为阳极且反应为:Li++e-═Li |
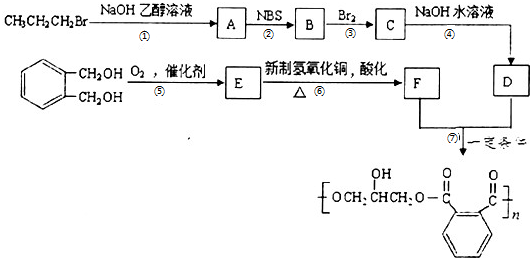
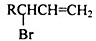
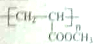 ,请设计合成路线(无机试剂及溶剂任选).注:合成路线的书写格式参照如下示例流程图:CH2=CH2$\stackrel{HBr}{→}$CH3CH2Br$→_{△}^{NaOH溶液}$CH3CH2OH.
,请设计合成路线(无机试剂及溶剂任选).注:合成路线的书写格式参照如下示例流程图:CH2=CH2$\stackrel{HBr}{→}$CH3CH2Br$→_{△}^{NaOH溶液}$CH3CH2OH.