题目内容
8.选用一种试剂除去下列各物质中的杂质(括号内为杂质),把所选试剂的化学式填在横线上,并写出离子方程式.(1)BaCl2(HCl)试剂BaCO3;离子方程式为BaCO3+2H+═Ba2++H2O+CO2↑
(2)CO(CO2)试剂NaOH溶液;离子方程式为2OH-+CO2═CO32-+H2O
(3)Fe SO4 (Cu SO4)Fe粉;离子方程式为Fe+Cu2+═Cu+Fe2+.
分析 (1)碳酸钡与氯化氢反应生成氯化钡,可选用BaCO3除去HCl;
(2)CO不与氢氧化钠溶液反应,而二氧化碳与氢氧化钠溶液反应,可用氢氧化钠溶液除去一氧化碳中的二氧化碳杂质;
(3)铜离子与铁粉反应生成硫酸亚铁和铜单质,据此可除去硫酸亚铁中的硫酸铜杂质.
解答 解:(1)氯化氢与碳酸钡反应生成氯化钡、二氧化碳气体和水,故可选用BaCO3除去HCl,反应的离子方程式为:BaCO3+2H+═Ba2++H2O+CO2↑,
故答案为:BaCO3;BaCO3+2H+═Ba2++H2O+CO2↑;
(2)一氧化碳为中性气体、二氧化碳是酸性气体,可选用NaOH溶液除去二氧化碳,反应离子方程式为:2OH-+CO2═CO32-+H2O,
故答案为:NaOH溶液、2OH-+CO2═CO32-+H2O;
(3)铁粉和硫酸铜能发生置换反应生成铜,同时生成硫酸亚铁,反应的离子方程式为:Fe+Cu2+═Cu+Fe2+.
故答案为:Fe粉;Fe+Cu2+═Cu+Fe2+.
点评 本题考查除杂方法及离子方程式的书写,题目难度中等,解决除杂问题时,抓住除杂质的必需条件(加入的试剂只与杂质反应,反应后不能引入新的杂质)是解题的关键,注意掌握离子方程式的书写原则.

练习册系列答案
相关题目
15.某消毒液的主要成分为NaClO,还含有一定量的NaOH,下列叙述正确的是( )
| A. | 用pH试纸测得该消毒液的pH约为12 | |
| B. | 该消毒液中,Fe3+、K+、NO${\;}_{3}^{-}$、CH3CHO可以大量共存 | |
| C. | 向该消毒液中滴入少量Na2SO3溶液,反应的离子方程为:SO${\;}_{3}^{2-}$+ClO-=Cl-+SO${\;}_{4}^{2-}$ | |
| D. | 向该消毒液中加入浓盐酸,每产生1mol Cl2,转移电子数约为2×6.02×1023 |
19.硅烷是一类最简单的有机硅化合物,其分子组成与烷烃相似,下列说法中错误的是( )
| A. | 硅烷的分子通式为SinH2n+2 | B. | 甲硅烷燃烧生成二氧化硅和水 | ||
| C. | 甲硅烷的密度大于甲烷 | D. | 甲硅烷的热稳定性强于甲烷 |
20.下列有机物的命名正确的是( )
| A. | CH2(OH)CH2CH2(OH) 丙三醇 | |
| B. | (CH3)3CCH2CH(C2H5)CH3 2,2,5-三甲基己烷 | |
| C. | 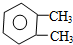 二甲苯 二甲苯 | |
| D. | 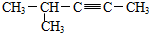 2-甲基-3-戊炔 2-甲基-3-戊炔 |
17.下列关于有机化合物的说法中,正确的是( )
| A. | 有机物都不是电解质 | |
| B. | 所有的有机化合物都很容易燃烧 | |
| C. | 有机物中一定含有C元素,也可含H、N、S等元素 | |
| D. | 易溶于汽油、酒精、苯等有机溶剂的物质一定是有机化合物 |
18.在120℃时,某混合烃和过量O2在一密闭容器中完全反应,恢复到120℃时,测知反应前后的压强没有变化,则该混合烃可能是( )
| A. | CH4和C2H4 | B. | CH4和C2H6 | C. | C2H4和C2H6 | D. | C3H4和C3H6 |