题目内容
12.设NA为阿伏伽德罗常数的值.下列说法正确的是( )| A. | 0.1mol Na2O2与足量的潮湿的二氧化碳反应转移的电子数为0.1NA | |
| B. | 1mol镁与足量O2或N2反应生成MgO或Mg3N2失去电子分别为2NA和3NA | |
| C. | 含NA个Na+的Na2O2溶于1L水中,Na+的物质的量浓度为1 mol/L | |
| D. | 某密闭容器中盛有0.2molN2和0.3molH2,在一定条件下充分反应,转移电子的数目为0.6 NA |
分析 A、过氧化钠和二氧化碳的反应为歧化反应;
B、镁反应后变为+2价;
C、将过氧化钠溶于1L水中后,溶液体积不再是1L;
D、合成氨的反应为可逆反应.
解答 解:A、过氧化钠和二氧化碳的反应为歧化反应,1mol过氧化钠转移1mol电子,则0.1mol过氧化钠转移0.1mol电子即0.1NA个,故A正确;
B、镁反应后变为+2价,故1mol镁失去2mol电子即2NA个,与产物无关,故B错误;
C、将过氧化钠溶于1L水中后,溶液体积不再是1L,故溶液中的钠离子的浓度不是1mol/L,故C错误;
D、合成氨的反应为可逆反应,不能进行彻底,则转移的电子数小于0.6NA个,故D错误.
故选A.
点评 本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,难度不大.

练习册系列答案
相关题目
2.短周期原子序数依次增大的主族元素R、T、Q、W、Y、Z具有如下信息:①R、Y原子的最外层电子数与电子层数相同;②Q是地壳中含量最高的元素,R与T的核电荷数之和等于Q的核电荷数;③W与R同主族,Z与Q同主族.下列说法正确的是( )
| A. | Q与Y组成的常见物质是一种两性物质,结构中含有共价键 | |
| B. | 已知WRZQ3溶液呈酸性,若将WRZQ3固体溶于水,能促进水的电离 | |
| C. | 元素Q与W形成的两种常见化合物中含有相同比例的阴、阳离子 | |
| D. | 元素T、Q、W、Y的原子半径大小为T<Q<Y<W |
3.25℃时,0.1mol/LMOH溶液的pH约为11,该溶液与0.1mol/L的硫酸溶液混合生成1molM2SO4时放出的热量为24.6kJ,又知稀硫酸的中和热为57.3kJ/mol,则MOH电离时的△H为( )
| A. | +45 kJ/mol | B. | +32.7 kJ/mol | C. | -45 kJ/mol | D. | 无法计算 |
20.下表是元素周期表的一部分,针对表中的①~⑩中元素,用元素符号或化学式填空回答以下问题:
(1)在这些元素中最活泼的非金属元素是F
(2)元素的最高价氧化物对应的水化物中酸性最强的是HClO4,碱性最强的是KOH
(3)呈两性的氢氧化物是Al(OH)3,其与③的最高价氧化物水化物反应的离子方程式为Al(OH)3+OH-=AlO2-+2H2O
(4)在③~⑦元素中,原子半径最大的是Na
(5)在⑦与⑩的单质中,化学性质较活泼的是Cl2,可用什么化学反应说明该事实(写出反应的化学方程式):2NaBr+Cl2=2NaCl+Br2.
| 主族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
| 二 | ① | ② | ||||||
| 三 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ||
| 四 | ⑨ | ⑩ |
(2)元素的最高价氧化物对应的水化物中酸性最强的是HClO4,碱性最强的是KOH
(3)呈两性的氢氧化物是Al(OH)3,其与③的最高价氧化物水化物反应的离子方程式为Al(OH)3+OH-=AlO2-+2H2O
(4)在③~⑦元素中,原子半径最大的是Na
(5)在⑦与⑩的单质中,化学性质较活泼的是Cl2,可用什么化学反应说明该事实(写出反应的化学方程式):2NaBr+Cl2=2NaCl+Br2.
2.下列生活常识与化学原理有关,其中说法错误的是( )
| A. | 加工后具有吸水性的植物纤维可用作食品干燥剂 | |
| B. | 服用阿司匹林出现水杨酸反应时,用NaHCO3溶液解毒 | |
| C. | 明矾水解形成氢氧化铝胶体能杀菌消毒,可用水的净化 | |
| D. | 硫酸亚铁补铁剂应与维生素C同服,是因为维生素C可以防止Fe2+被氧化 |
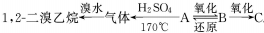 ,其中B可发生银镜反应,C跟石灰石反应产生能使石灰水变浑浊的气体;
,其中B可发生银镜反应,C跟石灰石反应产生能使石灰水变浑浊的气体;