题目内容
 Ⅰ.一定温度下,将3mol CO2和2mol H2混合于2L的密闭容器中,发生如下反应:C02(g)+H2(g)?CO(g)+H2O(g)
Ⅰ.一定温度下,将3mol CO2和2mol H2混合于2L的密闭容器中,发生如下反应:C02(g)+H2(g)?CO(g)+H2O(g)(1)该反应的化学平衡常数表达式K=
(2)已知在700℃时,该反应的平衡常数K1=0.6,在1000℃时,该反应的平衡常数K2=1.0,则该反应为
(3)在1000℃下,某时刻CO2的物质的量为2.0mol,则此时v(正)
Ⅱ.研究NO2、SO2、CO等大气污染气体的处理具有重要意义.
(1)已知反应:NO2(g)+SO2(g)?SO3(g)+NO(g)在一定条件下,将NO2与SO2以体积比1:2置于密闭容器中发生上述反应,下列能说明反映达到平衡状态的是
a.体系压强保持不变 b.混合气体颜色保持不变
c.SO3与NO的体积比保持不变 d.每消耗1mol SO3的同时生成1mol NO2
测得上述反应平衡时NO2与SO2体积比为1:6,则平衡常数K=
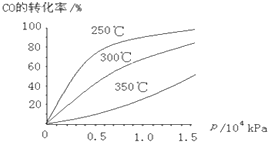
(2)CO可用于合成甲醇,反应方程式为CO(g)+2H2(g)?CH3OH(g).CO在不同温度下的平衡转化率与压强的关系如图所示.该反应△H
考点:转化率随温度、压强的变化曲线,化学平衡常数的含义,化学平衡的计算
专题:化学平衡专题
分析:Ⅰ、(1)化学平衡常数K=
;
(2)对于吸热反应,温度升高,化学反应的平衡常数会增大;
(3)根据浓度商与平衡常数判断反应方向,根据平衡常数计算反应的二氧化碳的量,再结合转化率计算二氧化碳的转化率.
Ⅱ、(1)根据化学平衡状态的特征:逆、定、动、变、等来判断化学反应是否达到平衡,据三行式以及化学平衡常数表达式计算化学平衡常数;
(2)从横坐标上一点,画一条平行于纵坐标的虚线,看相同压强下不同温度时CO的平衡转化率,温度越低转化率越低,说明,升温时平衡向逆向移动.
| 各个产物平衡浓度系数次方的乘积 |
| 各个反应物平衡浓度系数次方的乘积 |
(2)对于吸热反应,温度升高,化学反应的平衡常数会增大;
(3)根据浓度商与平衡常数判断反应方向,根据平衡常数计算反应的二氧化碳的量,再结合转化率计算二氧化碳的转化率.
Ⅱ、(1)根据化学平衡状态的特征:逆、定、动、变、等来判断化学反应是否达到平衡,据三行式以及化学平衡常数表达式计算化学平衡常数;
(2)从横坐标上一点,画一条平行于纵坐标的虚线,看相同压强下不同温度时CO的平衡转化率,温度越低转化率越低,说明,升温时平衡向逆向移动.
解答:
解:Ⅰ、(1)化学平衡常数K=
=
,故答案为:
;
(2)温度升高,化学反应的平衡常数增大,则该反应是吸热反应,故答案为:吸热;
(3)CO2(g)+H2(g)═CO(g)+H2O(g)
起始1.5 1 0 0
反应0.5 0.5 0.5 0.5
平衡1 0.5 0.5 0.5
浓度商Qc=
=0.5<1,则反应向正反应方向移动,所以v(正)>v(逆);
3mol CO2和2mol H2混合于2L的密闭容器中,则二氧化碳和氢气的起始浓度分别为1.5mol/L、1mol/L,在1 000℃下,某时刻CO2的物质的量为2.0mol,某时刻二氧化碳的浓度是1mol/L,设该温度下达到平衡时,反应的二氧化碳的物质的量浓度为x
CO2(g)+H2(g)═CO(g)+H2O(g)
起始:1.5 1 0 0
反应:x x x x
平衡:1.5-x 1-x x x
=1.0,x=0.6
二氧化碳的转化率=
×100%=40%,
故答案为:>;40%;
Ⅱ、(1)反应NO2(g)+SO2(g)?SO3(g)+NO(g)是反应前后气体分子数不变的反应,故体系的压强保持不变,故a不能说明反应已达到平衡状态;随着反应的进行,NO2的浓度减小,颜色变浅,故b可以说明反应已达平衡;SO3和NO都是生成物,比例保持1:1,故c不能作为平衡状态的判断依据;d中所述的两个速率都是逆反应速率,不能作为平衡状态的判断依据,故选b;
O2(g)+SO2(g) SO3(g)+NO(g)
SO3(g)+NO(g)
起始物质的体积 a 2a 0 0
转化物质的体积 x x x x
平衡物质的体积 a-x 2a-x x x
则
=
a-x,故x=
a,故平衡常数为=
=
≈2.67,故答案为:b;2.67或
;
(2)从横坐标上一点0.5处,画一条平行于纵坐标的虚线,看相同压强下不同温度时CO的平衡转化率,温度越低转化率越低,说明,升温时平衡向逆向移动.
第二问:工业生产要考虑速经济效益,要考虑速度和效率,压强越大需要的条件越高,花费越大.
故答案为:<;250℃、1.3×104kPa左右,CO的转化率已经很高,如果增加压强CO的转化率提高不大,而生产成本增加,得不偿失.
| 各个产物平衡浓度系数次方的乘积 |
| 各个反应物平衡浓度系数次方的乘积 |
| c(CO)?c(H2O) |
| c(CO2)?c(H2) |
| c(CO)?c(H2O) |
| c(CO2)?c(H2) |
(2)温度升高,化学反应的平衡常数增大,则该反应是吸热反应,故答案为:吸热;
(3)CO2(g)+H2(g)═CO(g)+H2O(g)
起始1.5 1 0 0
反应0.5 0.5 0.5 0.5
平衡1 0.5 0.5 0.5
浓度商Qc=
| 0.52 |
| 1×0.5 |
3mol CO2和2mol H2混合于2L的密闭容器中,则二氧化碳和氢气的起始浓度分别为1.5mol/L、1mol/L,在1 000℃下,某时刻CO2的物质的量为2.0mol,某时刻二氧化碳的浓度是1mol/L,设该温度下达到平衡时,反应的二氧化碳的物质的量浓度为x
CO2(g)+H2(g)═CO(g)+H2O(g)
起始:1.5 1 0 0
反应:x x x x
平衡:1.5-x 1-x x x
| x2 |
| (1.5-x)(1-x) |
二氧化碳的转化率=
| 0.6 |
| 1.5 |
故答案为:>;40%;
Ⅱ、(1)反应NO2(g)+SO2(g)?SO3(g)+NO(g)是反应前后气体分子数不变的反应,故体系的压强保持不变,故a不能说明反应已达到平衡状态;随着反应的进行,NO2的浓度减小,颜色变浅,故b可以说明反应已达平衡;SO3和NO都是生成物,比例保持1:1,故c不能作为平衡状态的判断依据;d中所述的两个速率都是逆反应速率,不能作为平衡状态的判断依据,故选b;
O2(g)+SO2(g)
 SO3(g)+NO(g)
SO3(g)+NO(g)起始物质的体积 a 2a 0 0
转化物质的体积 x x x x
平衡物质的体积 a-x 2a-x x x
则
| a-x |
| 2a-x |
| 1 |
| 6 |
| 4 |
| 5 |
| x2 |
| (a-x)(2a-x) |
| 8 |
| 3 |
| 8 |
| 3 |
(2)从横坐标上一点0.5处,画一条平行于纵坐标的虚线,看相同压强下不同温度时CO的平衡转化率,温度越低转化率越低,说明,升温时平衡向逆向移动.
第二问:工业生产要考虑速经济效益,要考虑速度和效率,压强越大需要的条件越高,花费越大.
故答案为:<;250℃、1.3×104kPa左右,CO的转化率已经很高,如果增加压强CO的转化率提高不大,而生产成本增加,得不偿失.
点评:本题考查了化学平衡常数的有关计算,明确化学平衡常数的表达式及其含义是解本题关键,会利用三段式法进行解答,会根据浓度商与平衡常数之间的关系式确定反应方向,题目难度中等.

练习册系列答案
相关题目
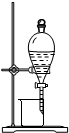
完成下列实验,所选装置正确的是( )
| A | B | C | D | |
| 实验 目的 |
检查装置气密性 | 实验室用纯碱和稀硫酸制备二氧化碳 | 用已知浓度的氢氧化钠溶液测定未知浓度盐酸 | 从碘的CCl4溶液中分离出碘 |
| 实验装置 | 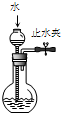 |
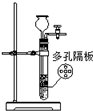 |
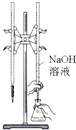 |
 |
| A、A | B、B | C、C | D、D |
一定量的锎(
Cf)是有用的中子源,在医学上常用作治疗恶性肿瘤的中子源.下列有关锎的说法错误的是( )
252 98 |
A、
| ||
B、
| ||
C、
| ||
| D、锎元素位于第6周期 |
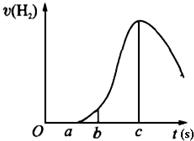 把在空气中久置的镁条7.2g投入盛有500mL 0.5mol?L-1硫酸溶液的烧杯中,镁条与硫酸反应产生氢气的速率与反应时间如图所示,回答下列问题:
把在空气中久置的镁条7.2g投入盛有500mL 0.5mol?L-1硫酸溶液的烧杯中,镁条与硫酸反应产生氢气的速率与反应时间如图所示,回答下列问题: