题目内容
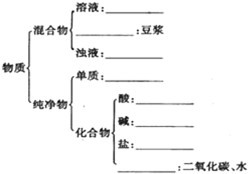 有下列物质:A.豆浆,B.食盐水,C.铁,D.硫酸,E.氢氧化钠固体,F.氯化钠,G.泥水,H.二氧化碳,I.水.请将它们的序号或所属类别填充到如图的横线上.(填写序号)
有下列物质:A.豆浆,B.食盐水,C.铁,D.硫酸,E.氢氧化钠固体,F.氯化钠,G.泥水,H.二氧化碳,I.水.请将它们的序号或所属类别填充到如图的横线上.(填写序号)属于电解质的是
考点:电解质与非电解质
专题:电离平衡与溶液的pH专题
分析:根据酸是能电离出的阳离子全部是H+的化合物;
碱是电离出的阴离子全部是OH-离子的化合物;
盐是电离出阳离子是金属阳离子或铵根离子、阴离子为酸根离子的化合物;
氧化物由两种元素组成,其中一种为氧元素的化合物,
分散质粒子的直径大小在1nm~100nm的是胶体,分散质粒子的直径大于100nm的是浊液,分散质粒子的直径小于1nm的是溶液.
在水溶液中或熔化状态下能导电的化合物为电解质,在水溶液中和熔化状态下都不能导电的化合物为非电解质;单质和混合物既不是电解质,也不是非电解质;
碱是电离出的阴离子全部是OH-离子的化合物;
盐是电离出阳离子是金属阳离子或铵根离子、阴离子为酸根离子的化合物;
氧化物由两种元素组成,其中一种为氧元素的化合物,
分散质粒子的直径大小在1nm~100nm的是胶体,分散质粒子的直径大于100nm的是浊液,分散质粒子的直径小于1nm的是溶液.
在水溶液中或熔化状态下能导电的化合物为电解质,在水溶液中和熔化状态下都不能导电的化合物为非电解质;单质和混合物既不是电解质,也不是非电解质;
解答:
解:A.豆浆分散质粒子的直径大小在1nm~100nm,属于胶体;
B.食盐水:NaCl的水溶液;
C.铁:由铁元素构成的单质;
D.H2SO4:电离出的阳离子全部是H+属于酸;
E.氢氧化钠固体:电离出的阴离子全部是OH-,属于碱;
F.纯碱的花学式为Na2CO3,由金属阳离子和酸根离子构成的盐;
G.泥水:由泥和水形成的浊液.
H.二氧化碳:由两种元素组成,其中一种为氧元素的化合物,属于氧化物;
I.水:由两种元素组成,其中一种为氧元素的化合物,属于氧化物;
故答案为:B;胶体;G;C;D;E;F;氧化物.
在水溶液中或熔化状态下能导电的化合物属于电解质,满足该条件达到有:D.硫酸,E.氢氧化钠固体,F.氯化钠,I.水;
非电解质在水溶液中和熔化状态下都不能导电的化合物,满足条件的有:H.二氧化碳;
单质和混合物既不是电解质,也不是非电解质,满足条件的有:A.豆浆,B.食盐水,C.铁,G.泥水;
故答案为:DEFI;H;ABCG.
B.食盐水:NaCl的水溶液;
C.铁:由铁元素构成的单质;
D.H2SO4:电离出的阳离子全部是H+属于酸;
E.氢氧化钠固体:电离出的阴离子全部是OH-,属于碱;
F.纯碱的花学式为Na2CO3,由金属阳离子和酸根离子构成的盐;
G.泥水:由泥和水形成的浊液.
H.二氧化碳:由两种元素组成,其中一种为氧元素的化合物,属于氧化物;
I.水:由两种元素组成,其中一种为氧元素的化合物,属于氧化物;
故答案为:B;胶体;G;C;D;E;F;氧化物.
在水溶液中或熔化状态下能导电的化合物属于电解质,满足该条件达到有:D.硫酸,E.氢氧化钠固体,F.氯化钠,I.水;
非电解质在水溶液中和熔化状态下都不能导电的化合物,满足条件的有:H.二氧化碳;
单质和混合物既不是电解质,也不是非电解质,满足条件的有:A.豆浆,B.食盐水,C.铁,G.泥水;
故答案为:DEFI;H;ABCG.
点评:本题考查酸碱盐以及氧化物、胶体、电解质与非电解质的概念及分类,题目难度不大,解答本题的关键把握相关概念以及物质的组成.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
已知有机物A、B、C之间存在如下转化关系:A+H2O→B+C(已配平).若MB=MC,且B溶液能使紫色石蕊溶液变红,且其含氧元素的质量分数为36.36%.则C的同分异构体的种数为( )
| A、6 | B、7 | C、8 | D、9 |
下列离子方程式正确的是( )
| A、NH4Cl溶液与NaOH溶液混合:OH-+NH4+═NH3?H2O |
| B、稀硫酸滴在铜片上:Cu+2H+═Cu2++H2↑ |
| C、将铝粉投入氢氧化钠溶液中:Al+2OH-═2AlO2- |
| D、NaHCO3溶液与盐酸混合:HCO3-+H+═CO32-+H2O |
 把在空气中久置的镁条7.2g投入盛有500mL 0.5mol?L-1硫酸溶液的烧杯中,镁条与硫酸反应产生氢气的速率与反应时间如图所示,回答下列问题:
把在空气中久置的镁条7.2g投入盛有500mL 0.5mol?L-1硫酸溶液的烧杯中,镁条与硫酸反应产生氢气的速率与反应时间如图所示,回答下列问题: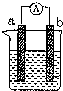 如图是某化学兴趣小组探究不同条件下化学能转变为电能的装置.请回答下列问题:
如图是某化学兴趣小组探究不同条件下化学能转变为电能的装置.请回答下列问题: