题目内容
有一无色透明溶液,欲确定是否含有下列离子:Na+、Mg2+、Al3+、Fe2+、NO3-、SO42-、Cl-、HCO3-、Cu2+,取该溶液实验如下:
①取少量该溶液,加几滴石蕊试液,溶液变红色
②取少量该溶液,浓缩,加Cu片和浓H2SO4,加热,有无色气体产生,后在空气中又变成红棕色
③取少量该溶液,加BaCl2溶液,有白色沉淀生成
④取③中上层清液,加AgNO3溶液,有白色沉淀生成,且不溶于HNO3
⑤取少量该溶液,加NaOH溶液,有白色沉淀生成,当NaOH过量时沉淀部分溶解
根据上述实验现象判断:
(1)溶液中肯定存在的离子是 .
(2)溶液中肯定不存在的离子是 .
(3)为进一步确定可能存在的离子,应该补充的实验是 .
①取少量该溶液,加几滴石蕊试液,溶液变红色
②取少量该溶液,浓缩,加Cu片和浓H2SO4,加热,有无色气体产生,后在空气中又变成红棕色
③取少量该溶液,加BaCl2溶液,有白色沉淀生成
④取③中上层清液,加AgNO3溶液,有白色沉淀生成,且不溶于HNO3
⑤取少量该溶液,加NaOH溶液,有白色沉淀生成,当NaOH过量时沉淀部分溶解
根据上述实验现象判断:
(1)溶液中肯定存在的离子是
(2)溶液中肯定不存在的离子是
(3)为进一步确定可能存在的离子,应该补充的实验是
考点:常见阳离子的检验,常见阴离子的检验
专题:物质检验鉴别题
分析:依据溶液无色,排除Fe2+、Cu2+;依据加几滴石蕊试液,溶液变红色,排除HCO3-;依据加Cu片和浓H2SO4,加热,有无色气体产生,后在空气中又变成红棕色,确定有NO3-;依据加BaCl2溶液,有白色沉淀生成,确定有:SO42-;依据取③中上层清液,加AgNO3溶液,有白色沉淀生成,且不溶于HNO3,不能确定是否含Cl-;依据加NaOH溶液,有白色沉淀生成,当NaOH过量时沉淀部分溶解,确定含有Mg2+、Al3+.
解答:
解:因为是无色透明溶液,Fe2+是浅绿色,故不含有,Cu2+是蓝色,故不含有;
①取少量该溶液,加几滴石蕊试液,溶液变红色,说明溶液显酸性,故不含有:HCO3-;
②取少量该溶液,浓缩,加Cu片和浓H2SO4,加热,有无色气体产生,后在空气中又变成红棕色,无色气体是NO,红色气体为NO2,故溶液中存在NO3-;
③取少量该溶液,加BaCl2溶液,有白色沉淀生成,故溶液中含有SO 42-;
④取③中上层清液,加AgNO3溶液,有白色沉淀生成,且不溶于HNO3不能确定是否含有Cl-,因为③中引入了氯离子;
⑤取少量该溶液,加NaOH溶液,有白色沉淀生成,当NaOH过量时沉淀部分溶解,镁离子与铝离子都生成沉淀,沉淀部分溶解,即氢氧化铝溶解,氢氧化镁不溶,故一定含有 Mg2+、Al3+.(1)依据以上分析,溶液中一定存在的离子是:Mg2+、Al3+、NO3-、SO42-,故答案为:Mg2+、Al3+、NO3-、SO42-;
(2)依据以上分析,溶液中一定不存在的离子是:Fe2+、HCO3-、Cu2+.,故答案为:Fe2+、HCO3-、Cu2+;
(3)不能确定是否存在的离子是Na+、Cl-,为进一步确定可能存在的离子,应该补充的实验是:另取该溶液少许于试管中加入硝酸酸化后,加入硝酸银溶液如有白色沉淀则含有Cl-;取该溶液做焰色反应实验如显黄色 则含有Na+;
故答案为:另取该溶液少许于试管中加入硝酸酸化后,加入硝酸银溶液如有白色沉淀则含有Cl-;取该溶液做焰色反应实验如显黄色 则含有Na+.
①取少量该溶液,加几滴石蕊试液,溶液变红色,说明溶液显酸性,故不含有:HCO3-;
②取少量该溶液,浓缩,加Cu片和浓H2SO4,加热,有无色气体产生,后在空气中又变成红棕色,无色气体是NO,红色气体为NO2,故溶液中存在NO3-;
③取少量该溶液,加BaCl2溶液,有白色沉淀生成,故溶液中含有SO 42-;
④取③中上层清液,加AgNO3溶液,有白色沉淀生成,且不溶于HNO3不能确定是否含有Cl-,因为③中引入了氯离子;
⑤取少量该溶液,加NaOH溶液,有白色沉淀生成,当NaOH过量时沉淀部分溶解,镁离子与铝离子都生成沉淀,沉淀部分溶解,即氢氧化铝溶解,氢氧化镁不溶,故一定含有 Mg2+、Al3+.(1)依据以上分析,溶液中一定存在的离子是:Mg2+、Al3+、NO3-、SO42-,故答案为:Mg2+、Al3+、NO3-、SO42-;
(2)依据以上分析,溶液中一定不存在的离子是:Fe2+、HCO3-、Cu2+.,故答案为:Fe2+、HCO3-、Cu2+;
(3)不能确定是否存在的离子是Na+、Cl-,为进一步确定可能存在的离子,应该补充的实验是:另取该溶液少许于试管中加入硝酸酸化后,加入硝酸银溶液如有白色沉淀则含有Cl-;取该溶液做焰色反应实验如显黄色 则含有Na+;
故答案为:另取该溶液少许于试管中加入硝酸酸化后,加入硝酸银溶液如有白色沉淀则含有Cl-;取该溶液做焰色反应实验如显黄色 则含有Na+.
点评:本题考查离子存在的判断,关键是明确题中信息的挖掘和应用,并能够熟悉离子不能共存的常见的原因,本题难度中等.

练习册系列答案
相关题目
(双选)常温下,下列各组离子一定可以大量共存的是( )
| A、强碱性溶液中:Na+、CO32-、SO32-、K+ |
| B、石蕊呈红色的溶液:ClO-、Na+、SO32-、Cl- |
| C、PH>7的溶液中:Mg2+、Br-、K+、Al3+ |
| D、加入Fe能放出H2的溶液中:Cl-、Mg2+、SO42-、K+ |
在下列给定条件的溶液中,一定能大量共存的离子组是( )
| A、加入Al能放出H2的溶液中:Mg2+、Cu2+、SO42-、NO3- |
| B、能使酚酞变红的溶液中:K+、Na+、Cl-、CO32- |
| C、无色透明的水溶液中:K+、Ba2+、I-、MnO4- |
| D、常温下,在c(H+)/c(OH-)=1×10-12的溶液中:Fe2+、Cu2+、Cl-、NO3- |

 物质A-E都是由下表中的离子组成的,常温下各物质从l mL稀释到1000mL,pH的变化如图l所示,其中A与D反应得到E.请回答:
物质A-E都是由下表中的离子组成的,常温下各物质从l mL稀释到1000mL,pH的变化如图l所示,其中A与D反应得到E.请回答: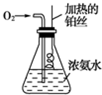 按如图所示的装置进行实验:
按如图所示的装置进行实验: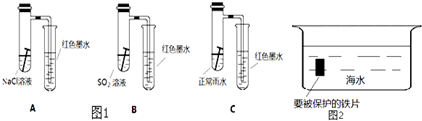

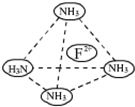 物质结构与性质A、B、C、D、E为原子序数依次增大的六种元素.已知:A是周期表中原子半径最小的元素,B的基态原子2p原子轨道上有3个未成对的电子,且B、C、E三种元素原子中未成对电子数之比为3:2:1,D原子核外有4个能级且均充满电子,D与E可形成DE2型化合物,F原子核外最外层只有1个电子,其余各层均充满电子.
物质结构与性质A、B、C、D、E为原子序数依次增大的六种元素.已知:A是周期表中原子半径最小的元素,B的基态原子2p原子轨道上有3个未成对的电子,且B、C、E三种元素原子中未成对电子数之比为3:2:1,D原子核外有4个能级且均充满电子,D与E可形成DE2型化合物,F原子核外最外层只有1个电子,其余各层均充满电子.