题目内容
 物质结构与性质A、B、C、D、E为原子序数依次增大的六种元素.已知:A是周期表中原子半径最小的元素,B的基态原子2p原子轨道上有3个未成对的电子,且B、C、E三种元素原子中未成对电子数之比为3:2:1,D原子核外有4个能级且均充满电子,D与E可形成DE2型化合物,F原子核外最外层只有1个电子,其余各层均充满电子.
物质结构与性质A、B、C、D、E为原子序数依次增大的六种元素.已知:A是周期表中原子半径最小的元素,B的基态原子2p原子轨道上有3个未成对的电子,且B、C、E三种元素原子中未成对电子数之比为3:2:1,D原子核外有4个能级且均充满电子,D与E可形成DE2型化合物,F原子核外最外层只有1个电子,其余各层均充满电子.回答下列问题:
(1)B、C、D三种元素的第一电离能由大到小的顺序为
(2)F在周期表中位于
(3)B、D、E三种元素中可形成XY3形化合物的化学式为
(4)A与B形成的化合物易溶解在A与C形成的化合物中,其原因是
(5)DC化合物熔点高于DE2的熔点,其原因是
(6)F2+与NH3形成配离子[F(NH3)4]2+,在[F(NH3)4]2+中,F2+位于正四面体中心,NH3位于正四面体的顶点,试在图中表示[F(NH3)4]2+中F2+与N之间的化学键.
考点:位置结构性质的相互关系应用
专题:元素周期律与元素周期表专题
分析:A是周期表中原子半径最小的元素,应为H元素,B的基态原子核外电子有7种运动状态,说明有7个电子,为N元素,B、C、E三种元素原子中未成对电子数之比为3:2:1,可推出C是O元素,由于D原子核外有4个能级且均充满电子,D与E可形成DE2型化合物,可推出E是Cl元素,D是Mg,再由F原子核外最外层只有1个电子,其余各层均充满电子,可推出F为Cu元素,与F同周期且未成对电子数最多的元素为Cr,结合对应元素对应的单质、化合物的性质以及题目要求解答该题.
解答:
解:A是周期表中原子半径最小的元素,应为H元素,B的基态原子核外电子有7种运动状态,说明有7个电子,为N元素,B、C、E三种元素原子中未成对电子数之比为3:2:1,可推出C是O元素,由于D原子核外有4个能级且均充满电子,D与E可形成DE2型化合物,可推出E是Cl元素,D是Mg,再由F原子核外最外层只有1个电子,其余各层均充满电子,可推出F为Cu元素,与F同周期且未成对电子数最多的元素为Cr,
(1)N和O在周期表相同周期,N的最外层为半充满结构,难以失去电子,第一电离能较大,为N>O>Mg,故答案为:N>O>Mg;
(2)F为Cu元素,价电子排布式为3d104s1,位于周期表ds区,与F同周期且未成对电子数最多的元素为Cr,故答案为:ds;3d104s1;Cr;
(3)B、E二种元素中可形成XY3形化合物的化学式为NCl3,N形成3个δ键,并有1个孤电子对,为sp3杂化,分子的空间构型为三角锥形,
故答案为:NCl3;sp3;三角锥形;
(4)A与B形成的化合物为氨气,A与C形成的化合物为水,两分子间易形成氢键,导致氨气极易溶于水,故答案为:两分子间易形成氢键;
(5)MgO化合物熔点高于MgCl2的熔点,原因是MgO的晶格能高于MgCl2,故答案为:MgO的晶格能高于MgCl2;
(6)F2+与N之间可形成配位键,可表示为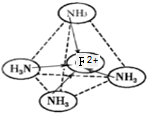 ,故答案为:
,故答案为: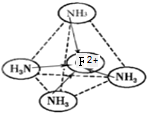 .
.
(1)N和O在周期表相同周期,N的最外层为半充满结构,难以失去电子,第一电离能较大,为N>O>Mg,故答案为:N>O>Mg;
(2)F为Cu元素,价电子排布式为3d104s1,位于周期表ds区,与F同周期且未成对电子数最多的元素为Cr,故答案为:ds;3d104s1;Cr;
(3)B、E二种元素中可形成XY3形化合物的化学式为NCl3,N形成3个δ键,并有1个孤电子对,为sp3杂化,分子的空间构型为三角锥形,
故答案为:NCl3;sp3;三角锥形;
(4)A与B形成的化合物为氨气,A与C形成的化合物为水,两分子间易形成氢键,导致氨气极易溶于水,故答案为:两分子间易形成氢键;
(5)MgO化合物熔点高于MgCl2的熔点,原因是MgO的晶格能高于MgCl2,故答案为:MgO的晶格能高于MgCl2;
(6)F2+与N之间可形成配位键,可表示为
 ,故答案为:
,故答案为: .
.
点评:本题应用元素周期表及周期律推断出各元素,并以此考查了元素的第一电离能,元素分区,价电子排布式,分子的空间构型,及中心原子的杂化类型,氢键及晶格能,及化学键,历年高考的必考题型,难度不大,解题的关键是要认真审读,挖掘题干隐含的信息,如“原子序数依次增大”.

练习册系列答案
相关题目
将等物质的量的A、B混合于2L的密闭容器中,发生下列反应:3A(g)+B(g)?xC(g)+2D(g),经2min后测得D的浓度为0.5mol/L,c(A):c(B)=3:5,以C表示的平均速率v(C)=0.25mol?L-1?min-1,下列说法正确的是( )
| A、反应速率v(B)=0.25 mol?L-1?min-1 |
| B、该反应方程式中,x=1 |
| C、2min时,A的物质的量为1.5mol |
| D、2min时,A的转化率为60% |
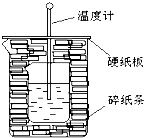 50ml0.50mol?L-1盐酸与50mL0.55mol?L-1NaOH溶液在如图所示的装置中进行中和反应.通过测定反应过程中放出的热量可计算中和热.回答下列问题:
50ml0.50mol?L-1盐酸与50mL0.55mol?L-1NaOH溶液在如图所示的装置中进行中和反应.通过测定反应过程中放出的热量可计算中和热.回答下列问题: