题目内容
12.a、b、c、d为短周期元素,a的原子中只有1个电子,b与a可形成多种有机化合物,c的单质是构成空气的主要成分,d元素的焰色反应呈黄色.下列叙述错误的是( )| A. | 简单离子半径:c>d | |
| B. | a、b、c、d中,d的原子半径最大 | |
| C. | a与b、c形成的化合物可能含有非极性键 | |
| D. | a与其它元素形成的化合物均为共价化合物 |
分析 a、b、c、d为短周期元素,a的原子中只有1个电子,a为H元素;b与a可形成多种有机化合物,b为C元素;c的单质是构成空气的主要成分,c为N或O,d元素的焰色反应呈黄色,d为Na,以此来解答.
解答 解:由上述分析可知,a为H,b为C,C为N或O,d为Na,
A.具有相同电子层结构的离子中原子序数大的离子半径小,则简单离子半径:c>d,故A正确;
B.电子层越多,原子半径越大,同周期从左向右原子半径减小,a、b、c、d中,d的原子半径最大,故B正确;
C.a与b、c形成的化合物可能含有非极性键,如氨基乙酸或乙醇中存在C-C非极性键,故C正确;
D.a与d形成离子化合物NaH,故D错误;
故选D.
点评 本题考查原子结构与元素周期律,为高频考点,把握元素化合物知识、原子结构、焰色反应来推断元素为解答的关键,侧重分析与应用能力的考查,注意规律性知识的应用,选项C为解答的难点,题目难度不大.

练习册系列答案
 开心快乐假期作业暑假作业西安出版社系列答案
开心快乐假期作业暑假作业西安出版社系列答案
相关题目
2.用NA表示阿伏加德罗常数的值.下列判断错误的是( )
| A. | NA个H+的质量为1 g | |
| B. | 2 L 0.5 mol/L Na2SO4溶液中含NA个Na+ | |
| C. | 32 g O2中含有2NA个氧原子 | |
| D. | 标准状况下,1 mol H2O中含有NA个分子 |
20. 元素R、X、T、Z、Q在元素周期表中的相对位置如表所示,其中R单质在暗处与H2剧烈化合并发生爆炸,则下列判断正确的是( )
元素R、X、T、Z、Q在元素周期表中的相对位置如表所示,其中R单质在暗处与H2剧烈化合并发生爆炸,则下列判断正确的是( )
 元素R、X、T、Z、Q在元素周期表中的相对位置如表所示,其中R单质在暗处与H2剧烈化合并发生爆炸,则下列判断正确的是( )
元素R、X、T、Z、Q在元素周期表中的相对位置如表所示,其中R单质在暗处与H2剧烈化合并发生爆炸,则下列判断正确的是( )| A. | 非金属性:X<T<Z | B. | 第一电离能:X<T<Z | ||
| C. | 气态氢化物的还原性:X<T<R | D. | 最高价氧化物的水化物酸性:Q<T<R |
7.已知:CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H
现在体积为1L的密闭容器中,充入CO2和H2.实验测得反应体系中物质的物质的量与时间关系如下表,
回答下列问题:
(1)表格中的n1=0.75mol
(2)0-5min内 v (H2)=0.3mol•L-1•min-1
(3)该条件下CO2的平衡转化率为75%.
现在体积为1L的密闭容器中,充入CO2和H2.实验测得反应体系中物质的物质的量与时间关系如下表,
| n(CO2) | n(H2) | n(CH3OH(g) | n(H2O(g) | |
| 0 | 1.00mol | 3.25mol | 0.00 | 0.00 |
| 5min | 0.50mol | 0.50mol | ||
| 10min | 0.25mol | 0.75mol | ||
| 15min | 0.25mol | n1 |
(1)表格中的n1=0.75mol
(2)0-5min内 v (H2)=0.3mol•L-1•min-1
(3)该条件下CO2的平衡转化率为75%.
17.下列关于某无色溶液中离子检验的操作、现象与结论对应正确的是( )
| 检验操作 | 现象 | 结论 | |
| A | 加入盐酸酸化的氯化钡 | 产生白色沉淀 | 一定有 SO42- |
| B | 加入氯水与四氯化碳 | 有机层呈紫色 | 一定有 I- |
| C | 加入足量稀盐酸 | 产生无色气体 | 一定有 CO32- |
| D | 加入硝酸银 | 产生白色沉淀 | 一定有 Cl- |
| A. | A | B. | B | C. | C | D. | D |
4.有机物R的结构简式如图所示.下列有关R的性质叙述正确的是( )
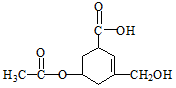

| A. | R的所有原子一定在同一平面上 | |
| B. | 在Ni催化和加热条件下,lmolR能与3molH2发生加成反应 | |
| C. | R既能与羧酸、醇反应,还能发生水解、加成和氧化反应 | |
| D. | 1molR与足量碳酸氢钠溶液反应,生成CO2的物质的量为2mol |
1.关于如图有机物说法正确的是( )


| A. | 该有机物的分子式为C7H7O3 | |
| B. | 1 mol该有机物只能与2 mol H2发生加成反应 | |
| C. | 该有机物在一定条件下能发生取代、氧化反应 | |
| D. | 该有机物的一种芳香族同分异构体能发生银镜反应 |
2.已知离子反应:Cu2++Zn→Cu+Zn2+,该反应证明Cu2+的氧化性强于( )
| A. | Zn2+ | B. | Zn | C. | Cu | D. | H+ |