题目内容
7.已知:CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H现在体积为1L的密闭容器中,充入CO2和H2.实验测得反应体系中物质的物质的量与时间关系如下表,
| n(CO2) | n(H2) | n(CH3OH(g) | n(H2O(g) | |
| 0 | 1.00mol | 3.25mol | 0.00 | 0.00 |
| 5min | 0.50mol | 0.50mol | ||
| 10min | 0.25mol | 0.75mol | ||
| 15min | 0.25mol | n1 |
(1)表格中的n1=0.75mol
(2)0-5min内 v (H2)=0.3mol•L-1•min-1
(3)该条件下CO2的平衡转化率为75%.
分析 由表格中数据可知,10min达到平衡,物质的量不变,则
CO2(g)+3H2(g)?CH3OH(g)+H2O(g)
开始 1.00 3.25 0 0
转化 0.75 2.25 0.75 0.75
平衡 0.25 1.00 0.75 0.75
结合v=$\frac{△c}{△t}$、转化率=$\frac{转化的量}{开始的量}$×100%来解答.
解答 解:由表格中数据可知,10min达到平衡,物质的量不变,则
CO2(g)+3H2(g)?CH3OH(g)+H2O(g)
开始 1.00 3.25 0 0
转化 0.75 2.25 0.75 0.75
平衡 0.25 1.00 0.75 0.75
(1)由上述分析可知,表格中的n1=0.75mol,故答案为:0.75mol;
(2)0-5min内 v (H2)=$\frac{\frac{(1.00mol-0.50mol)}{1L}}{5min}$×3=0.3 mol•L-1•min-1,故答案为:0.3 mol•L-1•min-1;
(3)该条件下CO2的平衡转化率为$\frac{0.75mol}{1.00mol}$×100%=75%,故答案为:75%.
点评 本题考查化学平衡的计算,为高频考点,把握表格中的数据、平衡三段法、速率及转化率的计算为解答的关键,侧重分析与计算能力的考查,注意速率之比等于化学计量数之比,题目难度不大.

 中考解读考点精练系列答案
中考解读考点精练系列答案| A. | 质量数是89 | B. | 质子数与中子数之差为50 | ||
| C. | 核外电子数是39 | D. | ${\;}_{39}^{89}$Y与${\;}_{39}^{90}$Y互为同位素 |
| A. | Na+、SO42-、Cl-、NO3- | B. | K+、Fe3+、Cl-、SCN- | ||
| C. | H+、Mg2+、SO42-、NO3- | D. | Al3+、K+、HS-、Na+ |
 H2 能在Cl2中燃烧生成 HCl,HCl也能在一定条件下分解为H2和Cl2. 图为H2、Cl2和HCl 三者相互转化的微观过程示意图,下列说法正确的是( )
H2 能在Cl2中燃烧生成 HCl,HCl也能在一定条件下分解为H2和Cl2. 图为H2、Cl2和HCl 三者相互转化的微观过程示意图,下列说法正确的是( )| A. | 过程 1 放热 | B. | 过程 2 吸热 | C. | 过程 3 放热 | D. | 过程 4 放热 |
| A. | 简单离子半径:c>d | |
| B. | a、b、c、d中,d的原子半径最大 | |
| C. | a与b、c形成的化合物可能含有非极性键 | |
| D. | a与其它元素形成的化合物均为共价化合物 |
| 实验事实 | 结论 | |
| A | 将燃烧的镁条放入CO2中能继续燃烧 | 还原性:Mg>C |
| B | Cl2的水溶液可以导电 | Cl2是电解质 |
| C | 将CO2气体通入苯酚钠溶液出现浑浊 | 酸性:H2CO3>苯酚 |
| D | 某无色溶液中加入氢氧化钠溶液并加热,产生的气体能使湿润红色石蕊试纸变蓝 | 该溶液一定有NH4+ |
| A. | A | B. | B | C. | C | D. | D |
| 选项 | 实验操作 | 现象 | 解释或结论 |
| A | 将铝片分別加入浓HNO3和NaOH浓溶液中 | NaOH浓溶液中的铝片溶解 | 铝不与浓HNO3反应 |
| B | 向紫色石蕊试液中通入足量二氧化硫 | 溶液由紫色变为红色 | 二氧化硫与水反应有酸性物质生成 |
| C | 将分别蘸有浓氨水和浓硝酸的两根玻璃棒相互靠近 | 有白烟生成 | 浓硝酸具有强氧化性 |
| D | 向待测液中加入盐酸酸化的硝酸钡溶液 | 有白色沉淀生成 | 待测液中含有SO42- |
| A. | A | B. | B | C. | C | D. | D |
| A. | N原子的轨道表示式: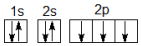 | B. | 氧化钠的分子式:Na2O | ||
| C. | 碳-14原子表示为:14C | D. | Na2S的电子式: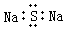 |
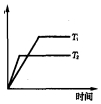 研究表明,在CuZnO2催化剂存在下,CO2和H2可发生两个平行反应,分别生成CH3OH和CO,反应的热化学方程式如下:
研究表明,在CuZnO2催化剂存在下,CO2和H2可发生两个平行反应,分别生成CH3OH和CO,反应的热化学方程式如下: