题目内容
17.下列关于某无色溶液中离子检验的操作、现象与结论对应正确的是( )| 检验操作 | 现象 | 结论 | |
| A | 加入盐酸酸化的氯化钡 | 产生白色沉淀 | 一定有 SO42- |
| B | 加入氯水与四氯化碳 | 有机层呈紫色 | 一定有 I- |
| C | 加入足量稀盐酸 | 产生无色气体 | 一定有 CO32- |
| D | 加入硝酸银 | 产生白色沉淀 | 一定有 Cl- |
| A. | A | B. | B | C. | C | D. | D |
分析 A.该白色沉淀可能为氯化银,原溶液中可能存在银离子,不一定含有硫酸根离子;
B.有机层呈紫色,说明生成碘;
C.该气体为二氧化碳,原溶液中可能含有碳酸氢根离子,不一定含有碳酸根离子;
D.加入硝酸银产生白色沉淀,沉淀可能为氯化银、硫酸银等.
解答 解:A.加入盐酸酸化的氯化钡生成沉淀,该白色沉淀可能为氯化银,原溶液中可能存在银离子,不一定含有硫酸根离子,应先加入盐酸,如无现象,再加入氯化钡检验,故A错误;
B.有机层呈紫色,说明生成碘,说明含有碘离子,故B正确;
C.向某溶液中加入稀盐酸,产生能使澄清石灰水变浑浊的无色无味气体,该气体为二氧化碳,但是原溶液中可能含有碳酸氢根离子,不一定含有碳酸根离子,故C错误;故C错误;
D.加入硝酸银产生白色沉淀,沉淀可能为氯化银、硫酸银等,不能确定是否含有氯离子,故D错误.
故选B.
点评 本题考查了常见离子的检验方法,为高频考点,题目难度中等,注意掌握常见离子的性质及检验方法,在检验离子存在时,需要排除干扰了,保证检验方案的严密性.

练习册系列答案
相关题目
7.下列关于离子共存或离子检验的说法正确的是( )
| A. | 某无色溶液中可能大量存在H+、Cl-、MnO4-、Al3+ | |
| B. | pH=2的溶液中可能大量存在Na+、NH4+、SiO32-、CO32- | |
| C. | 含有大量AlO2-的溶液中:K+、HCO3-、Br-、Na+可共存 | |
| D. | 在某钠盐溶液中含有等物质的量的Cl-、I-、AlO2-、CO32-、NO3-、SiO32-中若干种,当加入过量的盐酸产生气泡,溶液颜色变深,最终溶液中无沉淀,阴离子种数减少3种,则原溶液中一定有CO32- |
8.已知:2CO(g)+O2(g)═2CO2(g)△H=-566kJ/mol,下列说法正确的是( )
| A. | 2 L二氧化碳分解生成2 L一氧化碳和1 L氧气吸收576 kJ热量 | |
| B. | 恒压条件下生成物的总焓大于反应物的总焓 | |
| C. | 在相同条件下,2 mol一氧化碳与1 mol氧气的能量总和大于2 mol二氧化碳的能量 | |
| D. | 一氧化碳的燃烧热是566 kJ/mol |
5.已知:H-Cl和H-I键能分别为431KJ/mol和297KJ/mol,下列性质比较正确且可用键能数据说明原因的是( )
| A. | 稳定性:HI>HCl | B. | 熔、沸点:HI>HCl | ||
| C. | 同浓度的HI和HCl的酸性:HI>HCl | D. | 还原性:HI>HCl |
12.a、b、c、d为短周期元素,a的原子中只有1个电子,b与a可形成多种有机化合物,c的单质是构成空气的主要成分,d元素的焰色反应呈黄色.下列叙述错误的是( )
| A. | 简单离子半径:c>d | |
| B. | a、b、c、d中,d的原子半径最大 | |
| C. | a与b、c形成的化合物可能含有非极性键 | |
| D. | a与其它元素形成的化合物均为共价化合物 |
9.设NA为阿伏加德罗常数的值,下列说法正确的是( )
| A. | 100g 98%的浓硫酸中含有的氢原子数目为2NA | |
| B. | 常温下,2.7gAI与足量浓度为18mo1/L的浓硫酸反应时,转移的电子数为0.3NA | |
| C. | 标准状况下,22.4L的CCI4含有的CCl4分子数大于NA | |
| D. | 1 mol笨完全转化为环己烷,参与反应的碳碳双键数为3NA |
6.《本草图经》中关于绿矾的分解有如下描述:“绿矾形似朴消(Na2SO4•10H2O)而绿色,取此物置于铁板上,聚炭,封之囊袋,吹令火炽,其矾即沸,流出,色赤如融金汁者是真也.”对此段话的说明中肯定错误的是( )
| A. | 绿矾的化学式为FeSO4•7H2O | |
| B. | 绿矾分解过程中没有发生电子的转移 | |
| C. | “色赤”物质可能是Fe2O3 | |
| D. | 流出的液体中可能含有硫酸 |
7.Fe为26号元素,属于第四周期,最外层有2个电子.Fe3+最外层的电子数则为( )
| A. | 8 | B. | 13 | C. | 14 | D. | 18 |
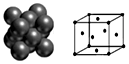 铁、铝、铜都是日常生活中常见的金属,它们的单质及其化合物在科学研究和工农业生产中具有广泛用途.请回答以下问题:
铁、铝、铜都是日常生活中常见的金属,它们的单质及其化合物在科学研究和工农业生产中具有广泛用途.请回答以下问题: ;NH4CuSO3中N、S、O三种元素的第一电离能由大到小的顺序为N>O>S(元素符号表示).
;NH4CuSO3中N、S、O三种元素的第一电离能由大到小的顺序为N>O>S(元素符号表示).