题目内容
3.Na、Al、Fe是生活中常见的金属元素.(1)工业上以铝土矿(主要成分Al2O3•3H2O)为原料生产铝,主要包括下列过程:
①将粉碎、筛选后的铝土矿溶解在氢氧化钠溶液中;
②通入过量二氧化碳使①所得溶液中析出氢氧化铝固体;③使氢氧化铝脱水生成氧化铝;④电解熔融氧化铝生成铝.
写出②所涉及离子反应方程式:AlO2-+2H2O+CO2═Al(OH)3↓+HCO3-,蒸干AlCl3溶液不能得到无水AlCl3,使SOCl2与AlCl3•6H2O混合并加热,可得到无水AlCl3,用化学方程式解释:6SOCl2+AlCl3•6H2O $\frac{\underline{\;\;△\;\;}}{\;}$12HCl+6SO2↑+AlCl3.
(2)铁在地壳中的含量约占5%左右.铁矿石的种类很多,重要的有磁铁矿石、赤铁矿石等.红热的铁能跟水蒸气反应,则其反应的化学方程式为3Fe+4H2O(g) $\frac{\underline{\;高温\;}}{\;}$Fe3O4+4H2.生成的黑色物质溶于酸后,加入KSCN溶液,见不到血红色产生,其原因是Fe3O4+8H+═Fe2++2Fe3++4H2O、Fe+2Fe3+=3Fe2+(用离子方程式解释).工业炼铁常用赤铁矿与Al在高温下反应制备,写出该反应的方程式:2Al+Fe2O3$\frac{\underline{\;\;△\;\;}}{\;}$2Fe+Al2O3.
(3)钠的化合物中,其中纯碱显碱性的原因是CO32-+H2O?HCO3-+OH-(用离子方程式解释),向饱和的纯碱溶液中通入过量的二氧化碳所产生现象晶体(或沉淀)析出,该物质是NaHCO3.(写化学式)
分析 (1)偏铝酸钠可以和过量二氧化碳反应生成氢氧化铝沉淀和碳酸氢钠,根据离子方程式的书写方法来书写;根据“SOCl2是一种液态化合物,与水发生剧烈的非氧化还原反应,生成两种有刺激性气味的气体、使SOCl2与AlCl3•6H2O混合并加热,可得到无水AlCl3”写出SOCl2与AlCl3•6H2O混合加热发生反应的化学方程式;
(2)红热的铁能与水蒸气发生反应,生成Fe3O4和一种可燃性气体,可燃气体为氢气;黑色的物质溶于酸后,加入KSCN,见不到血红色产生,说明溶液中无亚铁离子,可能是黑色固体物质中含有单质铁,或者溶于还原性的酸;铝热反应方程式为:2Al+Fe2O3=2Fe+Al2O3;
(3)钠的化合物中纯碱是强碱弱酸盐,碳酸钠水解而使溶液呈碱性;向饱和的纯碱溶于中通入过量的二氧化碳反应生成碳酸氢钠.
解答 解:(1)偏铝酸钠可以和过量二氧化碳反应生成氢氧化铝沉淀和碳酸氢钠,即AlO2-+2H2O+CO2═Al(OH)3↓+HCO3-;
SOCl2是一种液态化合物,与水发生剧烈的非氧化还原反应,生成两种有刺激性气味的气体,该两种气体应该为氯化氢和二氧化硫;使SOCl2与AlCl3•6H2O混合并加热,可得到无水AlCl3,反应生成、氯化铝、二氧化硫和氯化氢气体,所以SOCl2与AlCl3•6H2O混合加热发生反应的化学方程式:6SOCl2+AlCl3•6H2O $\frac{\underline{\;\;△\;\;}}{\;}$12HCl+6SO2↑+AlCl3,
故答案为:AlO2-+2H2O+CO2═Al(OH)3↓+HCO3-;6SOCl2+AlCl3•6H2O $\frac{\underline{\;\;△\;\;}}{\;}$12HCl+6SO2↑+AlCl3;
(2)红热的铁能与水蒸气发生反应,生成Fe3O4和氢气,反应为3Fe+4H2O(g) $\frac{\underline{\;高温\;}}{\;}$Fe3O4+4H2,黑色的物质溶于酸后,加入KSCN,见不到血红色产生,说明溶液中无亚铁离子,可能是黑色固体物质中含有单质铁,或者溶于还原性的酸,反应方程式为:Fe3O4+8H+═Fe2++2Fe3++4H2O,Fe+2Fe3+=3Fe2+,或者Fe3O4+8H++2I-=3Fe2++4H2O+I2,铝热反应方程式为:2Al+Fe2O3$\frac{\underline{\;\;△\;\;}}{\;}$2Fe+Al2O3,
故答案为:3Fe+4H2O(g) $\frac{\underline{\;高温\;}}{\;}$Fe3O4+4H2;Fe3O4+8H+═Fe2++2Fe3++4H2O、Fe+2Fe3+=3Fe2+或者Fe3O4+8H++2I-=3Fe2++4H2O+I2;2Al+Fe2O3$\frac{\underline{\;\;△\;\;}}{\;}$2Fe+Al2O3;
(3)纯碱是强碱弱酸盐,在纯碱溶液中CO32-易水解生成氢氧根离子:CO32-+H2O?HCO3-+OH-,导致溶液呈碱性;
向饱和的纯碱溶液中通入过量的二氧化碳,发生反应生成碳酸氢钠,反应的离子反应为:CO2+H2O+2Na++CO32-=2NaHCO3↓,则会有NaHCO3晶体(或沉淀)析出,
故答案为:CO32-+H2O?HCO3-+OH-;晶体(或沉淀)析出;NaHCO3.
点评 本题考查较为综合,涉及盐的水解原理、离子方程式、化学方程式书写等知识,题目难度中等,明确常见元素及其化合物性质为解答关键,试题培养了学生的分析能力及灵活应用能力.

 名校课堂系列答案
名校课堂系列答案 如图所示的原电池装置,X、Y 为两电极,电解质溶液为稀硫酸,外电路中的电子流向如图,对此装置的下列说法正确的是( )
如图所示的原电池装置,X、Y 为两电极,电解质溶液为稀硫酸,外电路中的电子流向如图,对此装置的下列说法正确的是( )| A. | 外电路的电流方向为:X→外电路→Y | |
| B. | 若两电极分别为 Zn 和碳棒,则 X 为碳棒,Y 为 Zn | |
| C. | 若两电极都是金属,则它们的活动性为 X>Y | |
| D. | X 极上发生的是还原反应,Y 极上发生的是氧化反应 |
| A. | pH=3的醋酸溶液与pH=11的NaOH溶液等体积混合,c(CH3COO-)>c(Na+)>c(H+)>c(OH-) | |
| B. | 4种pH相同的溶液:①CH3COONa ②C6H5ONa ③NaHCO3 ④NaOH,各溶液的物质的量浓度由大到小的顺序是③>②>①>④ | |
| C. | 0.1 mol•L-1HA(某酸)的pH=3,0.1 mol•L-1 BOH(某碱)的pH=13,则BA(盐)溶液的pH<7 | |
| D. | pH=2的盐酸与pH=l的硫酸溶液中c(H+)之比为2:1 |
| A. | 前2 min,D的平均反应速率为0.2 mol•L-1•min-1 | |
| B. | 此时,B的平衡转化率是40% | |
| C. | 增大该体系的压强,平衡不移动,化学平衡常数不变 | |
| D. | 增加B,平衡向右移动,B的平衡转化率增大 |
| A. | Na+、SO42-、Cl-、NO3- | B. | K+、Fe3+、Cl-、SCN- | ||
| C. | H+、Mg2+、SO42-、NO3- | D. | Al3+、K+、HS-、Na+ |
| A. | 2 L二氧化碳分解生成2 L一氧化碳和1 L氧气吸收576 kJ热量 | |
| B. | 恒压条件下生成物的总焓大于反应物的总焓 | |
| C. | 在相同条件下,2 mol一氧化碳与1 mol氧气的能量总和大于2 mol二氧化碳的能量 | |
| D. | 一氧化碳的燃烧热是566 kJ/mol |
 H2 能在Cl2中燃烧生成 HCl,HCl也能在一定条件下分解为H2和Cl2. 图为H2、Cl2和HCl 三者相互转化的微观过程示意图,下列说法正确的是( )
H2 能在Cl2中燃烧生成 HCl,HCl也能在一定条件下分解为H2和Cl2. 图为H2、Cl2和HCl 三者相互转化的微观过程示意图,下列说法正确的是( )| A. | 过程 1 放热 | B. | 过程 2 吸热 | C. | 过程 3 放热 | D. | 过程 4 放热 |
| A. | 简单离子半径:c>d | |
| B. | a、b、c、d中,d的原子半径最大 | |
| C. | a与b、c形成的化合物可能含有非极性键 | |
| D. | a与其它元素形成的化合物均为共价化合物 |
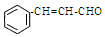 ),杏仁含苯甲醛(
),杏仁含苯甲醛( 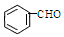 ),下列说法错误的是( )
),下列说法错误的是( )| A. | 肉桂醛和苯甲醛互为同系物 | |
| B. | 肉桂醛能发生加成反应、取代反应和加聚反应 | |
| C. | 可用新制氢氧化铜悬浊液检验肉桂醛分子中的含氧官能团 | |
| D. | 苯甲醛分子中所有原子可能位于同一平面内 |