题目内容
8.CH3-CH=CH-Cl,该有机物能发生( )①水解反应
②加成反应
③消去反应
④使溴水褪色
⑤光照条件下与氯气反应
⑥与硝酸银溶液产生白色沉淀
⑦聚合反应.
| A. | 以上反应均可发生 | B. | 只有⑦不能发生 | ||
| C. | 只有⑤不能发生 | D. | 只有⑥不能发生 |
分析 由结构可知,分子中含碳碳双键、-Cl,结合烯烃及卤代烃的性质来解答.
解答 解:含碳碳双键,可发生②加成反应、④使溴水褪色⑦聚合反应,
含-Cl,可发生①水解反应、③消去反应,
只有⑥与AgNO3溶液生成白色沉淀不能发生,因不能电离出氯离子,
含有甲基,在光照条件下可发生取代反应,
故选D.
点评 本题考查有机物的结构与性质,为高频考点,把握官能团与性质的关系为解答的关键,侧重分析与应用能力及烯烃、卤代烃性质的考查,题目难度不大.

练习册系列答案
 天天练口算系列答案
天天练口算系列答案
相关题目
18.若NA表示阿伏加德罗常数的值,下列说法正确的是( )
| A. | 在标准状况下,NA个水分子所占的体积约为22.4L | |
| B. | 5.6g铁与氯气完全反应,失去电子的数目为0.2NA | |
| C. | 1mol氯气发生化学反应,转移的电子数必为2NA | |
| D. | CH4的摩尔质量与NA个CH4分子的质量在数值上相等 |
19.足量的镁与一定质量的盐酸反应,由于反应速率太快,若要减慢反应速率,但不能影响产生氢气的总质量,可以加入下列物质中的是( )
| A. | H2O | B. | NaOH | C. | K2CO3 | D. | CH3COONa |
16.根据下列反应的化学方程式,试判断有关物质的还原性强弱顺序( )
I2+SO2+2H2O=4H++SO42-+2I-
2Fe2++Cl2=2Fe3++2Cl-
2Fe3++2I-=2Fe2++I2.
I2+SO2+2H2O=4H++SO42-+2I-
2Fe2++Cl2=2Fe3++2Cl-
2Fe3++2I-=2Fe2++I2.
| A. | I->Fe2+>Cl->SO2 | B. | Cl->Fe2+>SO2>I- | C. | Fe2+>I->Cl->SO2 | D. | SO2>I->Fe2+>Cl- |
3.已知A、B、C、D的原子序数都不超过18,它们的离子aA(n+1)+、bBn+、cC(n+1)-、dDn-具有相同的电子层结构,则下列说法正确的是( )
| A. | 原子序数:a>b>c>d | |
| B. | 离子半径:A(n+1)+>Bn+>C(n+1)->Dn- | |
| C. | 离子氧化性:A(n+1)+>Bn+离子还原性:C(n+1)->Dn- | |
| D. | C最高价氧化物的水化物的酸性比D的强 |
20.下列各组关于强电解质、弱电解质、非电解质的归类,完全正确的是( )
| 选项 | 强电解质 | 弱电解质 | 非电解质 |
| A | CaCO3 | H2SiO3 | 酒精 |
| B | NaCl | NH3 | BaSO4 |
| C | Fe | CH3COOH | 蔗糖 |
| D | HNO3 | Fe(OH)3 | H2O |
| A. | A | B. | B | C. | C | D. | D |
17.下列分散系中,明显与其他不同的一种是( )
| A. | 盐酸 | B. | 稀豆浆 | C. | NaOH溶液 | D. | FeCl3溶液 |
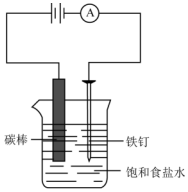 如图所示,回答下列问题:
如图所示,回答下列问题: