题目内容
16.根据下列反应的化学方程式,试判断有关物质的还原性强弱顺序( )I2+SO2+2H2O=4H++SO42-+2I-
2Fe2++Cl2=2Fe3++2Cl-
2Fe3++2I-=2Fe2++I2.
| A. | I->Fe2+>Cl->SO2 | B. | Cl->Fe2+>SO2>I- | C. | Fe2+>I->Cl->SO2 | D. | SO2>I->Fe2+>Cl- |
分析 同一自发进行的氧化还原反应中,氧化剂的氧化性大于氧化产物的氧化性,还原剂的还原性大于还原产物的还原性,据此分析解答.
解答 解:I2+SO2+2H2O=4H++SO42-+2I- 中还原剂是SO2、还原产物是HI,所以还原性SO2>I-;
2Fe2++Cl2=2Fe3++2Cl-中还原剂是Fe2+、还原产物是Cl-,所以还原性Fe2+>Cl-;
2Fe3++2I-=2Fe2++I2中还原剂是I-、还原产物是Fe2+,所以还原性I->Fe2+;
通过以上分析知,还原性强弱顺序是SO2>I->Fe2+>Cl-,
故选D.
点评 本题考查了还原性、氧化性强弱的比较,明确还原剂、氧化剂和还原产物、氧化产物的判断是解本题关键,难度不大.

练习册系列答案
 核心素养学练评系列答案
核心素养学练评系列答案 单元期中期末卷系列答案
单元期中期末卷系列答案
相关题目
7.设NA为阿伏加德罗常数的值,下列叙述正确的是( )
| A. | CO2通过Na2O2使其增重2.8g,反应中转移电子数为0.2NA | |
| B. | 3.36 L NO2与水充分反应转移的电子数目为0.1NA | |
| C. | 常温常压下,5.6g环丙烷和聚乙炔的混合物中含有的碳原子数为0.4NA | |
| D. | 2.0gH218O与D2O的混合物中所含中子数为NA |
4.下列叙述正确的是( )
| A. | 稀醋酸中加入少量醋酸钠能增大醋酸的电离程度 | |
| B. | 25℃时,等体积等物质的量浓度的硝酸与氨水混合后,溶液pH=7 | |
| C. | 25℃时,0.1 mol•L-1的硫化氢溶液比等浓度的硫化钠溶液的导电能力弱 | |
| D. | PH=2的酸HA溶液与PH=12的碱BOH溶液等体积混合后,所得溶液呈酸性,证明HA为强酸 |
11.按物质的组成进行分类,HNO3应属于①强酸;②氧化物;③含氧酸;④一元酸;⑤化合物( )
| A. | ①②③④⑤ | B. | ①③⑤ | C. | ①②③⑤ | D. | ①③④⑤ |
1.下列各组混合物中,可以用分液漏斗分离的是( )
| A. | 溴苯和水 | B. | 1,2-二溴乙烷和溴 | ||
| C. | 酒精和水 | D. | 正己烷和苯 |
8.CH3-CH=CH-Cl,该有机物能发生( )
①水解反应
②加成反应
③消去反应
④使溴水褪色
⑤光照条件下与氯气反应
⑥与硝酸银溶液产生白色沉淀
⑦聚合反应.
①水解反应
②加成反应
③消去反应
④使溴水褪色
⑤光照条件下与氯气反应
⑥与硝酸银溶液产生白色沉淀
⑦聚合反应.
| A. | 以上反应均可发生 | B. | 只有⑦不能发生 | ||
| C. | 只有⑤不能发生 | D. | 只有⑥不能发生 |
5.25℃时,在某物质的溶液中,由水电离出的c(H+)=1×10-amol/L,下列说法不正确的是( )
| A. | a>7时,水溶液一定不是中性 | B. | a>7时,水的电离受到抑制 | ||
| C. | a<7时,溶液的pH一定为a | D. | a>7时,溶液的pH一定为14-a |
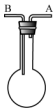 利用如图装置收集以下气体:①H2、②Cl2、③CH4、④HCl、⑤HBr
利用如图装置收集以下气体:①H2、②Cl2、③CH4、④HCl、⑤HBr