题目内容
 为了保持注水肉的色泽和水分,不法商赈向猪体内加入含有沙丁胺醇(如图)的胶类物质,该物质对人体危害很大,关于该物质以下说法不正确的是( )
为了保持注水肉的色泽和水分,不法商赈向猪体内加入含有沙丁胺醇(如图)的胶类物质,该物质对人体危害很大,关于该物质以下说法不正确的是( )| A、该物质属于芳香族化台物 |
| B、在一定条件下可发生取代反应和加成反应 |
| C、1mol该有机物与足量钠反应生成3NA个H2分子 |
| D、该有机物的分子式为C3H21NO3 |
考点:有机物的结构和性质
专题:有机物的化学性质及推断
分析:有机物含有酚羟基,可发生取代、氧化和显色反应,含有醇羟基,可发生取代、氧化反应,含有氨基,可与酸反应,以此解答该题.
解答:
解:A.分子中含有苯环,属于芳香族化台物,故A正确;
B.分子中含有羟基,可发生取代反应,含有苯环,可发生加成反应,故B正确;
C.分子中含有3个羟基,则1mol该有机物与足量钠反应生成1.5NA个H2分子,故C错误;
D.由有机物结构简式可知有机物分子式为C3H21NO3,故D正确.
故选C.
B.分子中含有羟基,可发生取代反应,含有苯环,可发生加成反应,故B正确;
C.分子中含有3个羟基,则1mol该有机物与足量钠反应生成1.5NA个H2分子,故C错误;
D.由有机物结构简式可知有机物分子式为C3H21NO3,故D正确.
故选C.
点评:本题考查有机物的结构和性质,为高考常见题型和高频考点,侧重于学生的分析能力的考查,注意把握有机物的结构特点和有机物官能团的性质,为解答该题的关键,难度不大.

练习册系列答案
 全能测控一本好卷系列答案
全能测控一本好卷系列答案
相关题目
 钢铁防腐方法有许多种,如图是其中的一种方法,描述正确的是( )
钢铁防腐方法有许多种,如图是其中的一种方法,描述正确的是( )| A、如图所示是牺牲阳极的阴极保护法 |
| B、铁闸门作阴极,发生还原反应 |
| C、电子流向:a→铁闸门,辅助电极→b |
| D、辅助电极上的反应:O2+2H2O+4e=4OH- |
下列反应的离子方程式书写正确的是( )
| A、用食醋除去水壶内的水垢:CaCO3+2H+═Ca2++CO2↑+H2O |
| B、用FeCl3溶液腐蚀铜线路板:Cu+Fe3+═Cu2++Fe2+ |
| C、FeBr2溶液中通入少量Cl2:2Br-+Cl2═Br2+2Cl- |
| D、在NaHCO3溶液中加入少量石灰水:2HCO3-+2OH-+Ca2+═CaCO3↓+CO32-+2H2O |
下列离子或分子组能大量共存,且满足相应要求的是( )
| A、Na+、K+、Ag+、NO3- 要求:逐滴滴加氨水先有沉淀产生,后沉淀消失 |
| B、Fe3+、NO3-、I-、HCO3- 要求:逐滴滴加盐酸立即有气体产生 |
| C、K+、AlO2-、Cl-、MnO4- 要求:无色澄清溶液 |
| D、NH4+、Al3+、SO42-、CH3COOH 要求:逐滴滴加NaOH溶液立刻有气体产生 |
下列说法正确的是( )
| A、水的离子积KW只与温度有关,但外加酸、碱、盐一定会影响水的电离程度 | ||||
| B、Ksp不仅与难溶电解质的性质和温度有关,还与溶液中相关离子的浓度有关 | ||||
C、常温下,在0.10mol?L-1的NH3?H2O溶液中加入少量NH4C1晶体,能使溶液的pH减小,
| ||||
| D、室温下,CH3COOH的Kα=1.7×10-5,NH3?H2O的Kb=1.7×10-5,CH3COOH溶液中的c (H+)与NH3?H2O中的c(OH-)相等 |
NA表示阿伏加德罗常数,下列说法正确的是( )
| A、30g SiO2含有NA个Si-O共价键 |
| B、1L 0.2mol?L-1 Al2(SO4)3溶液中的离子总数为NA |
| C、标准状况下,22.4L H2O所含原子个数大于3NA |
| D、含4mol HCl的浓盐酸跟足量MnO2加热反应可制得Cl2的分子数为NA |
下列实验装置能达到实验目的是( )
A、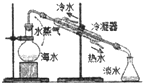 海水蒸馏 |
B、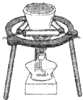 钾在空气中的燃烧 |
C、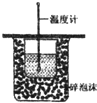 测定中和热 |
D、 牺牲阳极的阴极保护法 |
在下列各溶液中,离子一定能大量共存的是( )
| A、能与铝反应放出氢气的溶液中:K+、Al3+、Cl-、SO42- |
| B、水电离出来的c(H+)=10-12mol/L的溶液 Na+、Cl-、Br-、Ba2+ |
| C、所含溶质为Na2SO4的溶液 K+、CO32-、NO3-、Al3+ |
| D、室温下,pH=1的无色溶液中:Na+、Fe3+、NO3-、SO42- |


