题目内容
下列反应的离子方程式书写正确的是( )
| A、用食醋除去水壶内的水垢:CaCO3+2H+═Ca2++CO2↑+H2O |
| B、用FeCl3溶液腐蚀铜线路板:Cu+Fe3+═Cu2++Fe2+ |
| C、FeBr2溶液中通入少量Cl2:2Br-+Cl2═Br2+2Cl- |
| D、在NaHCO3溶液中加入少量石灰水:2HCO3-+2OH-+Ca2+═CaCO3↓+CO32-+2H2O |
考点:离子方程式的书写
专题:离子反应专题
分析:A.醋酸为弱酸,应写成化学式;
B.电荷不守恒;
C.还原性Fe2+>Br-,应先和Fe2+反应;
D.在NaHCO3溶液中加入少量石灰水,生成CaCO3和CO32-.
B.电荷不守恒;
C.还原性Fe2+>Br-,应先和Fe2+反应;
D.在NaHCO3溶液中加入少量石灰水,生成CaCO3和CO32-.
解答:
解:A.醋酸为弱酸,应写成化学式,应为CaCO3+2HAc═Ca2++2Ac-+CO2↑+H2O,故A错误;
B.用FeCl3溶液腐蚀铜线路板为Cu+2Fe3+═Cu2++2Fe2+,故B错误;
C.还原性Fe2+>Br-,FeBr2溶液中通入少量Cl2,离子方程式为2Fe2++Cl2═2Fe3++2Cl-,故C错误;
D.在NaHCO3溶液中加入少量石灰水,生成CaCO3和CO32-,反应的离子方程式为2HCO3-+2OH-+Ca2+═CaCO3↓+CO32-+2H2O,故D正确.
故选D.
B.用FeCl3溶液腐蚀铜线路板为Cu+2Fe3+═Cu2++2Fe2+,故B错误;
C.还原性Fe2+>Br-,FeBr2溶液中通入少量Cl2,离子方程式为2Fe2++Cl2═2Fe3++2Cl-,故C错误;
D.在NaHCO3溶液中加入少量石灰水,生成CaCO3和CO32-,反应的离子方程式为2HCO3-+2OH-+Ca2+═CaCO3↓+CO32-+2H2O,故D正确.
故选D.
点评:本题考查离子反应书写的正误判断,为高频考点,把握发生的化学反应及离子反应的书写方法为解答的关键,涉及与量有关的离子反应、水解反应等,综合性较强,题目难度不大.

练习册系列答案
 优学名师名题系列答案
优学名师名题系列答案
相关题目
下列说法正确的是( )
| A、PM2.5受到普遍的关注,因为PM2.5在空气中形成了气溶胶,富含大量的有毒、有害物质,对空气质量影响较大(PM2.5是指大气中直径接近于2.5×10-6m的颗粒物) |
| B、李比希燃烧法、钠熔法、铜丝燃烧法、纸层析法、元素分析仪都是元素定性分析法 |
| C、泡沫灭火器是最常见的灭火器之一,其内筒为塑料桶,盛有碳酸氢钠溶液;外筒为铁桶,外筒和内筒之间装有硫酸铝溶液 |
| D、“地沟油”经过加工处理后,可以用来制肥皂和生物柴油,可以实现厨余废物合理利用 |
t℃时,将100g某物质A的溶液蒸发掉10g水,恢复至t℃,析出2.5g晶体;再蒸发掉10g水,恢复至t℃,析出7.5g晶体.下列说法中正确的是( )
| A、t℃时原溶液是饱和溶液 |
| B、t℃时A的溶解度为75g |
| C、若A是CuSO4,则7.5g晶体中含水2.7g |
| D、原溶液中A的质量分数为40% |
 为了保持注水肉的色泽和水分,不法商赈向猪体内加入含有沙丁胺醇(如图)的胶类物质,该物质对人体危害很大,关于该物质以下说法不正确的是( )
为了保持注水肉的色泽和水分,不法商赈向猪体内加入含有沙丁胺醇(如图)的胶类物质,该物质对人体危害很大,关于该物质以下说法不正确的是( )| A、该物质属于芳香族化台物 |
| B、在一定条件下可发生取代反应和加成反应 |
| C、1mol该有机物与足量钠反应生成3NA个H2分子 |
| D、该有机物的分子式为C3H21NO3 |
下列解释实验过程或事实的反应方程式不正确的是( )
A、熔融烧碱时,不能使用氧化铝坩埚:Al2O3+2NaOH
| ||||
| B、刻制印刷电路时用FeCl3溶液作为“腐蚀液”:2Fe3++Cu=Cu2++2Fe2+ | ||||
C、打磨后的镁条置于沸水中,滴加酚酞溶液变红色:Mg+2H2O(g)
| ||||
| D、向KI溶液中滴加硫酸酸化的双氧水,溶液呈棕黄色:2I-+H2O2+2H+=I2+O2↑+2H2O |
XeF4在水中的反应为:6XeF4+12H2O═2XeO3+4Xe↑+24HF+3O2↑.下列说法中正确的是( )
| A、XeF4分子中各原子均达到8电子稳定结构 |
| B、XeF4分子中Xe的化合价为0价 |
| C、上述反应中氧化剂和还原剂的物质的量之比为2:3 |
| D、XeF4按上述方式水解,每生成4mol Xe,转移16mol电子 |
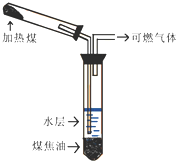 煤的干馏实验如图所示:
煤的干馏实验如图所示:


