题目内容
1.下列各组物质中,只用一种试剂不能鉴别的是( )| A. | 苯酚溶液、乙醇、己烯、四氯化碳 | B. | 甲酸、乙酸、乙醛、乙醇 | ||
| C. | 淀粉溶液、乙醇、苯、四氯化碳 | D. | 苯、甲苯、己烯、溴苯 |
分析 A.可利用溴水鉴别;
B.可利用氢氧化铜鉴别;
C.可利用碘水鉴别;
D.苯、甲苯的密度均比水小,甲苯、己烯均能被高锰酸钾氧化,一种试剂不能鉴别.
解答 解:A.可加入溴水鉴别,加入溴水,苯酚生成白色沉淀,乙醇和水混溶,己烯与溴水发生加成反应使其褪色,四氯化碳不溶于水,密度比水大,可鉴别,故A正确;
B.甲酸、乙酸、乙醛、乙醇分别与氢氧化铜反应的现象为:砖红色沉淀和蓝色溶液、蓝色溶液、砖红色沉淀、无现象,用一种试剂能鉴别,故B正确;
C.淀粉溶液、乙醇、苯、四氯化碳分别与碘水混合的现象为:蓝色、无现象、分层后有机层在上层、分层后有机层在下层,则能用一种试剂鉴别,故C正确;
D.苯、甲苯的密度均比水小,甲苯、己烯均能被高锰酸钾氧化,一种试剂不能鉴别,故D错误.
故选D.
点评 本题考查有机物的鉴别,为高频考点,侧重于学生的分析能力和综合运用化学知识的能力的考查,题目难度不大,注意把握物质的性质的异同.

练习册系列答案
相关题目
11.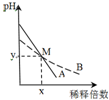 室温下,pH相差1的两种一元碱溶液A和B,分别加水稀释时,溶液的pH变化如图所示.下列说法正确的是( )
室温下,pH相差1的两种一元碱溶液A和B,分别加水稀释时,溶液的pH变化如图所示.下列说法正确的是( )
 室温下,pH相差1的两种一元碱溶液A和B,分别加水稀释时,溶液的pH变化如图所示.下列说法正确的是( )
室温下,pH相差1的两种一元碱溶液A和B,分别加水稀释时,溶液的pH变化如图所示.下列说法正确的是( )| A. | 稀释前,c(A)>10 c(B) | |
| B. | 中和等浓度等体积的盐酸时,B用的体积较多 | |
| C. | M点时A和B的浓度相等 | |
| D. | 在M点,A、B两种碱溶液中阳离子的物质的量浓度相等 |
12.有aXn+ 和bYm-两种元素的简单离子,若它们的电子层结构相同,则下列关系正确的是( )
| A. | b-a=n+m | B. | a-b=n-m | C. | 质子数Y>X | D. | 核电荷数Y<X |
16.下列说法全正确的是( )
①CH3-CH=CH2和CH2=CH2的最简式相同
②CH≡CH和C6H6含碳量相同
③碳原子数不同的直链烷烃一定是同系物
④正戊烷、异戊烷、新戊烷的沸点逐渐变低
⑤标准状况下,11.2L的己烷所含的分子数为0.5NA(NA为阿伏伽德罗常数)
⑥能够快速、微量、精确的测定相对分子质量的物理方法是核磁共振氢谱法.
①CH3-CH=CH2和CH2=CH2的最简式相同
②CH≡CH和C6H6含碳量相同
③碳原子数不同的直链烷烃一定是同系物
④正戊烷、异戊烷、新戊烷的沸点逐渐变低
⑤标准状况下,11.2L的己烷所含的分子数为0.5NA(NA为阿伏伽德罗常数)
⑥能够快速、微量、精确的测定相对分子质量的物理方法是核磁共振氢谱法.
| A. | ①②③④ | B. | ②③④⑥ | C. | ②③⑥ | D. | ③⑤⑥ |
6.下列说法正确的是( )
| A. | 将盐酸和醋酸钠溶液混合后溶液至中性,溶液中c(Na+)=c(Cl-) | |
| B. | 1 mol CH4分子中含有的共价键数目等于1 mol Na2O2固体中含有的离子总数 | |
| C. | 80℃的纯水的pH大于25℃的纯水的pH | |
| D. | 等体积、等pH的盐酸和醋酸与1mol/L的NaOH溶液完全中和,消耗的NaOH溶液体积后者多 |
13.下列关于金属晶体的叙述正确的是( )
| A. | 用铂金做首饰不能用金属键理论解释 | |
| B. | 固态和熔融时易导电,熔点在1 000℃左右的晶体可能是金属晶体 | |
| C. | Li、Na、K的熔点逐渐升高 | |
| D. | 金属导电和熔融电解质(或电解质溶液)导电的原理一样 |
10.能说明Cl比S的非金属性强的是( )
①Cl2比S容易与H2化合;
②Cl2能与S2-发生置换反应;
③酸性:HClO3>H2SO3;
④与Fe反应时,Cl2比S得电子数目多;
⑤Cl2比S单质熔、沸点低
⑥酸性:HCl>H2S.
①Cl2比S容易与H2化合;
②Cl2能与S2-发生置换反应;
③酸性:HClO3>H2SO3;
④与Fe反应时,Cl2比S得电子数目多;
⑤Cl2比S单质熔、沸点低
⑥酸性:HCl>H2S.
| A. | 只有④ | B. | ①②④ | C. | ①②③ | D. | ①②③④⑤ |
11.某由C、H、O元素组成的有机物球棍结构模型如图所示,下列说法中不正确的是( ) 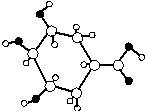

| A. | 该有机物不含苯环 | |
| B. | 分子式为C7H12O4 | |
| C. | 能与NaHCO3溶液反应生成CO2 | |
| D. | 1mol该有机物与足量的金属钠反应产生2molH2 |
 ;D所在族元素的氢化物中,稳定性最强的是(填化学式)H2O.
;D所在族元素的氢化物中,稳定性最强的是(填化学式)H2O.