题目内容
13.下列关于金属晶体的叙述正确的是( )| A. | 用铂金做首饰不能用金属键理论解释 | |
| B. | 固态和熔融时易导电,熔点在1 000℃左右的晶体可能是金属晶体 | |
| C. | Li、Na、K的熔点逐渐升高 | |
| D. | 金属导电和熔融电解质(或电解质溶液)导电的原理一样 |
分析 A、金属具有导电性、导热性,具有金属光泽,均有金属键有关;
B、固体或熔融状态易导电,可能为金属晶体;
C、Li、Na、K随原子序数逐渐增大,金属键减弱,熔点依次降低;
D、金属导电是靠自由移动的电子,电解质导电是靠自由移动的离子;
解答 解:A、用铂金做首饰,是因为有金属光泽,金属具有光泽是因为自由电子能够吸收可见光,能用金属键理论知识解释,故A错误;
B、金属晶体中有电子,能导电,大多数在常温下为固体,熔点较高,所以固体或熔融状态易导电,熔点在1000℃左右可能属于金属晶体,故B正确;
C、碱金属元素的单质,原子序数越大,原子半径越大,金属键越弱,熔沸点越低,则单质熔点:Li>Na>K,故C错误;
D、金属导电是靠自由移动的电子,电解质导电是靠自由移动的离子,导电的原理不一样,故D错误;
故选B.
点评 本题主要考查了金属晶体性质以及金属熔点的判断等,难度不大,注意对应知识的掌握.

练习册系列答案
相关题目
4.下列各组离子能在溶液中大量共存的是( )
| A. | HCO3-、Na+、OH-、K+ | B. | CO32-、Ba2+、K+、NO3- | ||
| C. | Ba2+、OH-、Cl-、Na+ | D. | CO32-、Na+、NO3-、H+ |
1.下列各组物质中,只用一种试剂不能鉴别的是( )
| A. | 苯酚溶液、乙醇、己烯、四氯化碳 | B. | 甲酸、乙酸、乙醛、乙醇 | ||
| C. | 淀粉溶液、乙醇、苯、四氯化碳 | D. | 苯、甲苯、己烯、溴苯 |
8.与0H?具有相同质子数和电子数的粒子是( )
| A. | F? | B. | C1? | C. | NH3 | D. | H2O |
18.常温下,向20mL 0.5mol•L-1的CH3COOH溶液中逐滴滴加0.5mol•L-1的NaOH溶液,滴定曲线如图.相关分析正确的是( )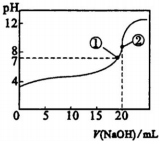

| A. | 滴加至①时,c(Na+)=c(CH3COO-),酸碱恰好完全反应 | |
| B. | 滴加至②时,c(OH-)-c(H+)=c(CH3COOH) | |
| C. | 滴定中,$\frac{c(C{H}_{3}CO{O}^{-})}{c({H}^{+})}$逐渐减小 | |
| D. | 滴定中.c(CH3COOH)与c(CH3 C00-)之和保持不变 |
5.有两种气态烷烃的混合物,在标准状况下密度为1.16g•L-1,则关于此混合物组成的说法正确的是( )
| A. | 一定有乙烷 | B. | 一定有丙烷 | ||
| C. | 可能是乙烷和丙烷的混合物 | D. | 可能是甲烷和丁烷的混合物 |
3.利用下列反应不能制得括号中纯净物质的是( )
| A. | 等物质的量的氯气与乙烷在光照条件下反应(氯乙烷) | |
| B. | 乙烯与氯气反应(1,2-二氯乙烷) | |
| C. | 液溴与苯用溴化铁作催化剂反应(溴苯) | |
| D. | 乙烯与水反应(乙醇) |