题目内容
 已知氯水中有如下平衡:Cl2+H2O?HCl+HClO.常温下在一个容积为50mL的针筒(如图所示,活塞可自由滑动,针筒上有刻度)里吸人40mLCl2和10mL H2O.
已知氯水中有如下平衡:Cl2+H2O?HCl+HClO.常温下在一个容积为50mL的针筒(如图所示,活塞可自由滑动,针筒上有刻度)里吸人40mLCl2和10mL H2O.(1)针筒中可观察到的现象是
(2)若将此针筒长时间放置在有日光的地方,最终可能观察到的现象是
(3)用化学平衡的观点解释(2)的现象:
考点:氯气的化学性质
专题:卤族元素
分析:(1)氯气溶于水,氯水呈黄绿色;
(2)氯水呈在反应Cl2+H2O?HCl+HClO,而且次氯酸见光分解生成氧气,次氯酸的浓度减小,平衡正向移动;
(3)结合(2)来解释分析.
(2)氯水呈在反应Cl2+H2O?HCl+HClO,而且次氯酸见光分解生成氧气,次氯酸的浓度减小,平衡正向移动;
(3)结合(2)来解释分析.
解答:
解:(1)氯气溶于水,氯水呈黄绿色,所以现象为:液体上方黄绿色气体体积减小,液体逐渐变为黄绿色,故答案为:液体上方黄绿色气体体积减小,液体逐渐变为黄绿色;
(2)氯水呈在反应Cl2+H2O?HCl+HClO,而且次氯酸见光分解生成氧气,次氯酸的浓度减小,平衡正向移动,现象为:液体上方气体体积增大,颜色为无色,并且液体中黄绿色消失,故答案为:液体上方气体体积增大,颜色为无色,并且液体中黄绿色消失;
(3)氯水呈在反应Cl2+H2O?HCl+HClO,而且次氯酸见光分解生成氧气,次氯酸的浓度减小,平衡正向移动,
故答案为:因为生成的次氯酸会分解产生氧气,(但是气体体积不会达到40ml,应该是20ml左右)使生成物浓度减小,平衡右移.
(2)氯水呈在反应Cl2+H2O?HCl+HClO,而且次氯酸见光分解生成氧气,次氯酸的浓度减小,平衡正向移动,现象为:液体上方气体体积增大,颜色为无色,并且液体中黄绿色消失,故答案为:液体上方气体体积增大,颜色为无色,并且液体中黄绿色消失;
(3)氯水呈在反应Cl2+H2O?HCl+HClO,而且次氯酸见光分解生成氧气,次氯酸的浓度减小,平衡正向移动,
故答案为:因为生成的次氯酸会分解产生氧气,(但是气体体积不会达到40ml,应该是20ml左右)使生成物浓度减小,平衡右移.
点评:本题考查氯气的化学性质,较好的考查了学生分析信息、应用知识解决问题的能力.

练习册系列答案
相关题目
下列根据实验现象所得出的结论中,正确的是( )
| A、某物质焰色反应呈黄色,结论:该物质是钠盐 |
| B、无色试液加入NaOH溶液,加热产生的气体使红色石蕊试纸变蓝,结论:试液中含NH3 |
| C、无色溶液中加入BaCl2溶液有白色沉淀产生,再加盐酸,沉淀不消失,结论:原溶液一定含有SO42- |
| D、无色溶液中加入稀盐酸产生无色无味气体,该气体能使澄清石灰水变浑浊,结论:原溶液可能含有CO32- |
把2.27gNaHCO3和Na2CO3?10H2O组成的混合物溶于水配成100ml溶液,其中C(Na+)=0.2mol?L-1,若将等质量的该混合物加热至恒重,所得固体质量为( )
| A、0.84g |
| B、1.06g |
| C、1.43g |
| D、2.27g |
在酸性溶液中,能大量共存的离子是( )
| A、Mg2+、AlO22+、NO3-、Cl- |
| B、Al3+、Fe2+、Cl-、SO42- |
| C、K+、Na+、Cl-、HCO3- |
| D、Na+、Ba2+、NO3-、SO42- |
水溶液中能大量共存的一组离子是( )
| A、Ba2+、Na+、Cl-、OH- |
| B、Fe2+、H+、SO42-、NO3- |
| C、Na+、Mg2+、Cl-、CO32- |
| D、K+、Fe3+、NO3-、SCN- |
下列有关溶液中粒子浓度的关系式中,正确的是( )
| A、pH相同的①CH3COONa ②NaHCO3 ③NaAlO2三份溶液中的c(Na+):③>②>① |
| B、0.1mol?L-1某二元弱酸强碱盐NaHA溶液中:c(Na+)=2c(A2-)+c(HA-)+c(H2A) |
| C、如图中a点溶液中各离子浓度的关系是:c(OH-)=c(H+)+c(CH3COO-)+2c(CH3COOH) |
D、如图中pH=7时:c(Na+)>c(CH3COO-)>c(OH-)=c(H+)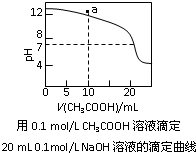 |
下列说法正确的是( )
| A、一定条件下,增加反应物的量,必加快反应速率 |
| B、升高温度对放热反应会减慢反应速率,而对吸热反应才会加快反应速率 |
| C、增大压强,对所有反应都会加快反应速率 |
| D、使用催化剂会加快反应速率 |
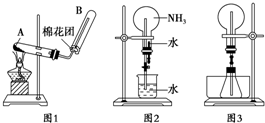 如图1为实验室制取氨的实验装置.
如图1为实验室制取氨的实验装置.