题目内容
Cu2S与一定浓度的HNO3反应,生成Cu(NO3)2、CuSO4、NO2、NO和H2O,当NO2和NO的物质的量为2:1时,则反应中Cu2S与被还原的HNO3的物质的量之比为( )
| A、1:6 | B、1:7 |
| C、1:8 | D、1:9 |
考点:氧化还原反应的计算
专题:计算题
分析:Cu2S与一定浓度的HNO3反应中,Cu2S中铜元素由+1价被氧化为+2价、硫元素由-2价被氧化为+6价,硝酸起氧化剂与酸的作用,起氧化剂作用HNO3中氮元素被还原为NO2和NO,起酸作用的硝酸生成Cu(NO3)2.令NO2和NO的物质的量分别为2mol、1mol,根据电子转移守恒计算参加反应的Cu2S的物质的量,被还原的硝酸的物质的量等于NO2和NO的物质的量之和,以此解答该题.
解答:
解:Cu2S与一定浓度的HNO3反应中,Cu2S中铜元素由+1价被氧化为+2价、硫元素由-2价被氧化为+6价,硝酸起氧化剂与酸的作用,起氧化剂作用HNO3中氮元素被还原为NO2和NO,
令NO2和NO的物质的量分别为2mol、1mol,根据电子转移守恒可知:
n(Cu2S)×[6-(-2)+1×2]=2mol×(5-4)+1mol×(5-2),解得n(Cu2S)=0.5mol.
被还原的硝酸的物质的量等于NO2和NO的物质的量之和,为3mol,
则被还原的硝酸的物质的量等于NO2和NO的物质的量之和,0.5mol:3mol=1:6,
故选A.
令NO2和NO的物质的量分别为2mol、1mol,根据电子转移守恒可知:
n(Cu2S)×[6-(-2)+1×2]=2mol×(5-4)+1mol×(5-2),解得n(Cu2S)=0.5mol.
被还原的硝酸的物质的量等于NO2和NO的物质的量之和,为3mol,
则被还原的硝酸的物质的量等于NO2和NO的物质的量之和,0.5mol:3mol=1:6,
故选A.
点评:本题考查化学方程式的有关计算,为高频考点,侧重于学生的分析能力和计算能力的考查,利用电子转移守恒与元素守恒计算是关键,转移守恒思想在氧化还原反应计算中的运用,难度不大.

练习册系列答案
 培优三好生系列答案
培优三好生系列答案 优化作业上海科技文献出版社系列答案
优化作业上海科技文献出版社系列答案
相关题目
下列变化不能用勒夏特列原理解释的是( )
| A、工业生产硫酸的过程中使用过量的氧气,以提高二氧化硫的转化率 |
| B、H2、I2(g)混合气体加压后颜色变深 |
| C、红棕色的NO2加压后颜色先变深再变浅 |
| D、实验室用排饱和食盐水的方法收集氯气 |
0.4mol Na2SO3恰好被0.1mol氧化剂X2O72-氧化生成Na2SO4,则元素X在还原产物中的化合价为( )
| A、+6 | B、+3 | C、+2 | D、0 |
能影响水的电离平衡,并使溶液中的c(H+)>c(OH-)的措施是( )
| A、向纯水中投入一小块金属钠 |
| B、将水加热煮沸 |
| C、向水中加入Na2CO3 |
| D、向水中加入NH4Cl |
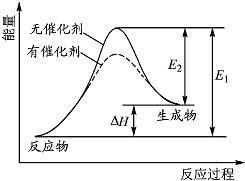 2HI(g)?H2(g)+I2(g)反应过程中能量变化如图所示(图中E1表示正反应的活化能,E2表示逆反应的活化能).下列有关叙述正确的是( )
2HI(g)?H2(g)+I2(g)反应过程中能量变化如图所示(图中E1表示正反应的活化能,E2表示逆反应的活化能).下列有关叙述正确的是( )| A、升高温度,反应速率增大,△H减小 |
| B、升高温度,不影响活化分子百分数 |
| C、催化剂能降低该反应的活化能 |
| D、逆反应的活化能等于正反应的活化能 |
如图是某同学从化学试剂商店买回的硫酸试剂标签上的部分内容.下列说法正确的( ) 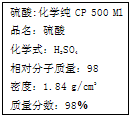

| A、该硫酸的物质的量浓度为9.2 mol/L |
| B、12gC与足量该硫酸共热反应,生成标准状况下气体体积为44.8L |
| C、1 mol Fe与足量的该硫酸反应产生2 g氢气 |
| D、配制200 mL 4.6 mol/L的稀硫酸需取该硫酸50 mL |
 已知氯水中有如下平衡:Cl2+H2O?HCl+HClO.常温下在一个容积为50mL的针筒(如图所示,活塞可自由滑动,针筒上有刻度)里吸人40mLCl2和10mL H2O.
已知氯水中有如下平衡:Cl2+H2O?HCl+HClO.常温下在一个容积为50mL的针筒(如图所示,活塞可自由滑动,针筒上有刻度)里吸人40mLCl2和10mL H2O.