题目内容
12.向2L密闭容器中通入amol气体A和bmol气体B,在一定条件下发生反应:xA(g)+yB(g)?pC(g)+qD(g)
已知:平均反应速率vC=$\frac{1}{2}$vA;反应2min时,A的浓度减少了$\frac{1}{3}$,B的物质的量减少了$\frac{a}{2}$mol,有amolD生成.回答下列问题:
(1)反应2min内,vA=$\frac{a}{12}$mol/(L•min),vB=$\frac{a}{8}$mol/(L•min);
(2)化学方程式中,x=2、y=3、p=1、q=6;
(3)反应平衡时,D为2amol,则B的转化率为$\frac{a}{b}$.
分析 (1)反应2min 时,A的浓度减少了$\frac{1}{3}$,则△c(A)=$\frac{1}{3}$×$\frac{amol}{2L}$=$\frac{1}{6}$amol/L,再根据v=$\frac{△c}{△t}$计算用A、B表示的反应速率;
(2)根据浓度据转化之比等于化学计量数之比;
(3)根据方程式计算消耗B的物质的量,B的转化率=$\frac{B的转化量}{B的初始量}$×100%计算.
解答 解:(1)反应2min 时,A的浓度减少了$\frac{1}{3}$,则△c(A)=$\frac{1}{3}$×$\frac{amol}{2L}$=$\frac{1}{6}$amol/L,则v(A)=$\frac{\frac{1}{6}mol/L}{2min}$=$\frac{a}{12}$(L•min);B的物质的量减少了$\frac{a}{2}$mol,则△c(B)=$\frac{\frac{a}{2}mol}{2L}$=$\frac{a}{4}$mol/L,v(B)=$\frac{\frac{a}{4}mol/L}{2min}$=$\frac{a}{8}$mol/(L•min);
故答案为:$\frac{a}{12}$mol/(L•min);$\frac{a}{8}$mol/(L•min);
(2)根据(1),△c(A)=$\frac{1}{6}$amol/L,△c(B)=$\frac{a}{4}$mol/L,由题vC=$\frac{1}{2}$vA;则△c(C)=$\frac{1}{2}$△c(A)=$\frac{a}{12}$
mol/L,△c(C)=$\frac{amol}{2L}$=$\frac{a}{2}$mol/L,则x:y:p:q=$\frac{1}{6}$a:$\frac{1}{4}$a:$\frac{1}{12}$a:$\frac{1}{2}$a=2::1:6;
故答案为:x=2,y=3,p=1,q=6;
(3)反应达到平衡时,D为2amol,由方程式2A(g)+3B(g)=C(g)+6D(g)可知消耗的B为2amol×$\frac{3}{6}$
=amol,故B的转化率为$\frac{a}{b}$;
故答案为:$\frac{a}{b}$.
点评 本题考查化学平衡的计算、反应速率计算,题目难度中等,根据反应速率关系以及物质的量的转化关系判断反应的化学方程式是解答该题的关键.

 名师伴你成长课时同步学练测系列答案
名师伴你成长课时同步学练测系列答案| A. | 转移溶液后未洗涤烧杯和玻璃棒就直接定容 | |
| B. | 移液前容量瓶中有少量蒸馏水 | |
| C. | 在容量瓶中进行定容时俯视刻度线 | |
| D. | 定容后把容量瓶倒转摇匀,发现液面低于刻度,再补充几滴水至刻度 |
(1)一定温度下,在两个容积均为2L的密闭容器中,分别发生反应:CO2 (g)+3H2(g)?CH3OH g)+H2O(g)△H=-49.0kJ/mol.相关数据如下:
| 容器 | 甲 | 乙 |
| 反应物投入量 | 1mol CO2(g)和3mol H2(g) | 1mol CH3OH(g)和1mol H2O(g) |
| 平衡时c(CH3OH) | c1 | c2 |
| 平衡时能量变化 | 放出29.4kJ | 吸收 a kJ |
②若甲中反应10s时达到平衡,则用CO2来表示甲中反应从开始到平衡过程中的平均反应速率是0.03mol/(L•S)
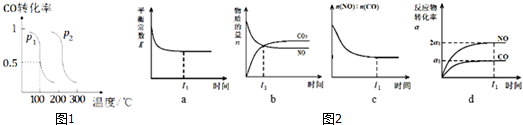
(2)压强为p1时,向体积为1L的密闭容器中充入b mol CO 和2b mol H2,发生反应CO (g)+2H2(g)?CH3OH(g).平衡时CO的转化率与温度、压强的关系如图1所示.请回答:①该反应属于放(填“吸”或“放”)热反应;p1 <p2(填“>”、“<”或“=”)
②100℃时,该反应的平衡常数K=$\frac{1}{{b}^{2}}$(用含b的代数式表示).
(3)一定条件下,治理汽车尾气的反应是2NO(g)+2CO(g)?2CO2(g)+N2(g)△H<0.在恒温恒容的密闭容器中通入n(NO):n(CO)=1:2的混合气体,发生上述反应.下列图象正确且能说明反应在进行到t1时刻一定达到平衡状态的是cd(选填字母).
| 1 | NaCl | NaHCO3 | NH4Cl |
| 10℃ | 35.8 | 8.15 | 33.0 |
| 45℃ | 37.0 | 14.0 | 50.0 |
工业制硝酸也是氨气重要用途之一,反应如下:
4NH3+5O2→4NO+6H2O 2NO+O2→2NO2 3NO2+H2O→2HNO3+NO
设空气中氧气的体积分数为0.20,氮气的体积分数为0.80.
(2)a mol NO完全转化为HNO3理论上需要氧气0.75amol;为使NH3恰好完全氧化为NO,氨-空气混合气体中氨的体积分数(用小数表示)为0.14.
(3)20.0mol NH3用空气氧化,产生混合物的组成为:NO 18.0mol、O2 12.0mol、N2 150.0mol和一定量硝酸,以及其他成分(高温下NO与O2不化合).计算氨转化为HNO3的转化率.
(写出简要计算过程)
| A. | 在限量范围内使用不会对人体造成危害 | |
| B. | 只有不法商贩才使用食品添加剂 | |
| C. | 不使用食品添加剂的纯天然食品最安全 | |
| D. | 食品添加剂就是为食品好卖出 |
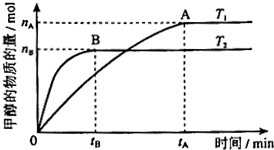 科学家利用太阳能分解水生成的氢气在催化剂作用下与二氧化碳反应生成甲醇.已知H2(g)、CO(g)和CH3OH(l)的燃烧热△H分别为-285.8kJ•mol-1、-283.0kJ•mol-1和-726.5kJ•mol-1.
科学家利用太阳能分解水生成的氢气在催化剂作用下与二氧化碳反应生成甲醇.已知H2(g)、CO(g)和CH3OH(l)的燃烧热△H分别为-285.8kJ•mol-1、-283.0kJ•mol-1和-726.5kJ•mol-1.