题目内容
下列实验方案正确且能达到相应实验预期目的是( )
A、 配置一定物质的量浓度的硫酸溶液 |
B、 检验装置的气密性 |
C、 从碘水中分离碘单质 |
D、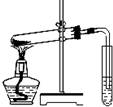 探究碳酸氢钠的热稳定性 |
考点:化学实验方案的评价
专题:实验评价题
分析:A.不能在容量瓶中稀释;
B.关闭止水夹,利用液面差检验气密性;
C.从碘水中分离碘单质,应利用萃取;
D.碳酸氢钠分解生成水,试管口不能向上倾斜.
B.关闭止水夹,利用液面差检验气密性;
C.从碘水中分离碘单质,应利用萃取;
D.碳酸氢钠分解生成水,试管口不能向上倾斜.
解答:
解:A.不能在容量瓶中稀释,应在烧杯中稀释、冷却后转移到容量瓶中,故A错误;
B.关闭止水夹,利用导管中液面与烧瓶中液面差在一段时间内不变来检验气密性,故B正确;
C.从碘水中分离碘单质,应利用萃取,而图中为蒸发,故C错误;
D.碳酸氢钠分解生成水,试管口不能向上倾斜,应略向下倾斜,故D错误;
故选B.
B.关闭止水夹,利用导管中液面与烧瓶中液面差在一段时间内不变来检验气密性,故B正确;
C.从碘水中分离碘单质,应利用萃取,而图中为蒸发,故C错误;
D.碳酸氢钠分解生成水,试管口不能向上倾斜,应略向下倾斜,故D错误;
故选B.
点评:本题考查化学实验方案的评价,为高频考点,涉及溶液的配制、混合物分离提纯、气密性检查、性质实验等,侧重化学反应原理及实验装置图的考查,注意实验操作性、评价性分析,题目难度不大.

练习册系列答案
相关题目
下列有关化学实验操作正确的是( )
A、 闻气味 |
B、 量取液体 |
C、 将乙醇与水分离 |
D、 检查装置的气密性 |
下图所示的实验操作,不能达到相应目的是( )
A、 干燥Cl2 |
B、 检验K2CO3中的K+ |
C、 证明氨气极易溶于水 |
D、 实验室制氨气 |
常温下,下列溶液中的微粒浓度关系正确的是( )
| A、新制氯水中加入固体NaOH:c(Na+)=c(Cl-)+c(ClO-)+c(OH-) |
| B、pH=8.3的NaHCO3溶液:c(Na+)>c(HCO3-)>c(CO32-)>c(H2CO3) |
| C、0.2mol?L-1 CH3COOH溶液与0.1mol?L-1 NaOH溶液等体积混合:2c(H+)-2c(OH-)=c(CH3COO-)-c(CH3COOH) |
| D、pH=11的氨水与pH=3的盐酸等体积混合:c(Cl-)=c(NH4+)>c(OH-)=c(H+) |
在下列四种反应条件下,锌和硫酸反应产生H2速率最慢的是( )
| A、20℃时,将锌片放入0.01 mol/L的稀硫酸中 |
| B、20℃时,将锌片放入0.1 mol/L的稀硫酸中 |
| C、50℃时,将锌片放入0.01 mol/L的稀硫酸中 |
| D、50℃时,将锌片放入0.1 mol/L的稀硫酸中 |
下列离子或分子在无色溶液中能大量共存的一组是( )
| A、Fe2+、OH-、Cl2 |
| B、Ag+、Cl-、SO42- |
| C、Na+、SO42-、NO3- |
| D、Al3+、NO3-、NH3?H2O |
设NA表示阿伏加德罗常数.下列叙述正确的是( )
| A、常温常压下,22g CO2中含有NA个C=O键 |
| B、标准状况下,将22.4L氯化氢气体溶于足量水中,溶液中含有的氯化氢分子数为NA |
| C、常温常压下,22.4L N2和O2的混合气体中含有的分子数目为NA |
| D、9g重水含有的电子数为5NA |