题目内容
设NA表示阿伏加德罗常数.下列叙述正确的是( )
| A、常温常压下,22g CO2中含有NA个C=O键 |
| B、标准状况下,将22.4L氯化氢气体溶于足量水中,溶液中含有的氯化氢分子数为NA |
| C、常温常压下,22.4L N2和O2的混合气体中含有的分子数目为NA |
| D、9g重水含有的电子数为5NA |
考点:阿伏加德罗常数
专题:阿伏加德罗常数和阿伏加德罗定律
分析:A.二氧化碳中含有2个碳氧双键,22g二氧化碳的物质的量为0.5mol,含有1mol碳氧双键;
B.氯化氢为强电解质,溶液中不存在氯化氢分子;
C.常温常压下,不能使用标况下的气体摩尔体积计算混合气体的物质的量;
D.重水中含有10个电子,9g重水的物质的量为0.45mol,含有4.5mol电子.
B.氯化氢为强电解质,溶液中不存在氯化氢分子;
C.常温常压下,不能使用标况下的气体摩尔体积计算混合气体的物质的量;
D.重水中含有10个电子,9g重水的物质的量为0.45mol,含有4.5mol电子.
解答:
解:A.22g二氧化碳的物质的量为0.5mol,0.5mol二氧化碳中含有1mol碳氧双键,含有NA个C=O键,故A正确;
B.氯化氢强电解质,溶液中完全电离,溶于水后不存在氯化氢分子,故B错误;
C.不是标准状况下,题中条件无法计算混合气体的物质的量,故C错误;
D.9g重水的物质的量为0.45mol,0.45mol重水中含有4.5mol电子,含有的电子数为4.5NA,故D错误;
故选A.
B.氯化氢强电解质,溶液中完全电离,溶于水后不存在氯化氢分子,故B错误;
C.不是标准状况下,题中条件无法计算混合气体的物质的量,故C错误;
D.9g重水的物质的量为0.45mol,0.45mol重水中含有4.5mol电子,含有的电子数为4.5NA,故D错误;
故选A.
点评:本题考查阿伏加德罗常数的有关计算和判断,题目难度中等,注意掌握好以物质的量为中心的各化学量与阿伏加德罗常数的关系,注意明确标况下气体摩尔体积的使用条件,选项D为易错点,注意重水的摩尔质量及含有的电子数.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
设NA为阿伏加德罗常数,下列叙述中正确的是( )
| A、c(H+)=0.1mol/L的甲酸溶液中,HCOO-和H+数目之和为0.1NA |
| B、标准状况下,3.36L乙烯中含有的极性键数为0.60NA |
| C、1L 0.2mol/L的Fe2(SO4)3溶液中含0.4NA个Fe3+离子 |
| D、1mol油酸含有的双键数目约为NA |
下列实验方案正确且能达到相应实验预期目的是( )
A、 配置一定物质的量浓度的硫酸溶液 |
B、 检验装置的气密性 |
C、 从碘水中分离碘单质 |
D、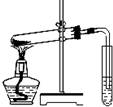 探究碳酸氢钠的热稳定性 |
室温下,向10mL,pH=12的某碱溶液中加入10mL pH=2的盐酸,充分反应后滴入酚酞试液,溶液变红,则此碱一定是( )
| A、弱碱 | B、一元强碱 |
| C、多元强碱 | D、任何强碱 |
废旧计算机的某些部件含有Zn、Fe、Cu、Ag、Pt(铂)、Au(金)等金属,经物理方法初步处理后,加入足量稀盐酸充分反应,再过滤,所得的固体中不应有的金属是( )
| A、Cu Ag |
| B、Zn Fe |
| C、Pt Cu |
| D、Ag Au |
在下列各组溶液中,离子一定能大量共存的是( )
| A、0.1 mol/L NaClO溶液:Fe2+、K+、I-、Cl- | ||
| B、通入足量CO2后的溶液中:Na+、C6H5O-、CH3COO-、HCO3- | ||
| C、加入铝粉能产生氢气的溶液中:NH4+、Fe2+、NO3-、SO42- | ||
D、
|

