题目内容
常温下,下列溶液中的微粒浓度关系正确的是( )
| A、新制氯水中加入固体NaOH:c(Na+)=c(Cl-)+c(ClO-)+c(OH-) |
| B、pH=8.3的NaHCO3溶液:c(Na+)>c(HCO3-)>c(CO32-)>c(H2CO3) |
| C、0.2mol?L-1 CH3COOH溶液与0.1mol?L-1 NaOH溶液等体积混合:2c(H+)-2c(OH-)=c(CH3COO-)-c(CH3COOH) |
| D、pH=11的氨水与pH=3的盐酸等体积混合:c(Cl-)=c(NH4+)>c(OH-)=c(H+) |
考点:离子浓度大小的比较
专题:盐类的水解专题
分析:A.溶液中存在电荷守恒,根据电荷守恒判断;
B.pH=8.3的NaHCO3溶液中,碳酸氢根离子水解程度大于电离程度;
C.二者混合时,溶液中的溶质是等物质的量浓度的CH3COOH和CH3COONa,溶液中存在物料守恒和电荷守恒;
D.pH=11的氨水与pH=3的盐酸等体积混合,氨水过量导致溶液呈碱性.
B.pH=8.3的NaHCO3溶液中,碳酸氢根离子水解程度大于电离程度;
C.二者混合时,溶液中的溶质是等物质的量浓度的CH3COOH和CH3COONa,溶液中存在物料守恒和电荷守恒;
D.pH=11的氨水与pH=3的盐酸等体积混合,氨水过量导致溶液呈碱性.
解答:
解:A.溶液中存在电荷守恒,根据电荷守恒得c(H+)+c(Na+)=c(Cl-)+c(ClO-)+c(OH-),所以c(Na+)<c(Cl-)+c(ClO-)+c(OH-),故A错误;
B.pH=8.3的NaHCO3溶液中,碳酸氢根离子水解程度大于电离程度,则c(CO32-)<c(H2CO3),故B错误;
C.二者混合时,溶液中的溶质是等物质的量浓度的CH3COOH和CH3COONa,依据溶液中物料守恒得2c(Na+)=c(CH3COOH)+c(CH3COO-),根据电荷守恒得c(Na+)+c(H+)=c(OH-)+c(CH3COO-),所以得2c(H+)-2c(OH-)=c(CH3COO-)-c(CH3COOH),故C正确;
D.pH=11的氨水与pH=3的盐酸等体积混合,氨水过量导致溶液呈碱性,则c(OH-)>c(H+),根据电荷守恒得c(Cl-)<c(NH4+),故D错误;
故选C.
B.pH=8.3的NaHCO3溶液中,碳酸氢根离子水解程度大于电离程度,则c(CO32-)<c(H2CO3),故B错误;
C.二者混合时,溶液中的溶质是等物质的量浓度的CH3COOH和CH3COONa,依据溶液中物料守恒得2c(Na+)=c(CH3COOH)+c(CH3COO-),根据电荷守恒得c(Na+)+c(H+)=c(OH-)+c(CH3COO-),所以得2c(H+)-2c(OH-)=c(CH3COO-)-c(CH3COOH),故C正确;
D.pH=11的氨水与pH=3的盐酸等体积混合,氨水过量导致溶液呈碱性,则c(OH-)>c(H+),根据电荷守恒得c(Cl-)<c(NH4+),故D错误;
故选C.
点评:本题考查了离子浓度大小比较,根据溶液中溶质的性质及溶液的酸碱性再结合物料守恒、电荷守恒来分析解答,易错选项是C,注意采用代入法分析,题目难度中等.

练习册系列答案
相关题目
如图为番茄电池,下列说法正确的是( )


| A、一段时间后,锌片质量会变大 |
| B、铜电极附近会出现蓝色 |
| C、电子由铜通过导线流向锌 |
| D、铜电极是该电池的正极 |
下列反应的离子方程式书写正确的是( )
| A、等体积等物质的量浓度的氢氧化钡溶液与碳酸氢铵溶液混合:Ba2++2OH-+NH4++HCO3-═BaCO3↓+NH3?H2O+H2O |
| B、氢氧化铁溶于氢碘酸溶液:Fe(OH)3+3H+═Fe3++3H2O |
| C、能使pH试纸显深红色的溶液,Fe3+、Cl-、Ba2+、I-能大量共存 |
| D、已知电离平衡常数:H2CO3>HClO>HCO3-,向NaClO溶液中通入少量CO2的离子方程式:2ClO-+CO2+H2O═2HClO+CO32- |
25℃时,下列各溶液中有关微粒的物质的量浓度关系正确的是( )
| A、在0.1 mol?L-1 Na2S溶液中:2c(Na+)=c(S2-)+c(HS-)+c(H2S) |
| B、pH=2的醋酸溶液与pH=12的NaOH溶液等体积混合:c(Na+)+c(H+)=c(OH-)+c(CH3COO-) |
| C、向0.1mol?L-1盐酸与0.1mol?L-1 K2CO3溶液等体积混合:c(K+)>c(Cl-)>c(HCO3-)>c(OH-)>c(H+) |
| D、向0.1mol?L-1 NH4HSO4溶液中滴加NaOH至溶液恰好呈中性:c(Na+)>c(NH4+)>c(SO42-)>c(OH-)=c(H+) |
下列实验方案正确且能达到相应实验预期目的是( )
A、 配置一定物质的量浓度的硫酸溶液 |
B、 检验装置的气密性 |
C、 从碘水中分离碘单质 |
D、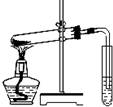 探究碳酸氢钠的热稳定性 |
废旧计算机的某些部件含有Zn、Fe、Cu、Ag、Pt(铂)、Au(金)等金属,经物理方法初步处理后,加入足量稀盐酸充分反应,再过滤,所得的固体中不应有的金属是( )
| A、Cu Ag |
| B、Zn Fe |
| C、Pt Cu |
| D、Ag Au |



