��Ŀ����
A��B��C��D��E���Ƕ�����Ԫ�أ�ԭ��������������C��D��E����ͬһ���ڣ�C��B�ɰ�ԭ�Ӹ�����2��l��1��1�ֱ��γ��������ӻ�������ң�A��ij�ֺ��ؿ����ڿ����ϼ�������������E�ǵؿ��к�����ߵĽ���Ԫ�أ�
����������Ϣ�ش��������⣺
��1��DԪ�������ڱ��е�λ���� �������ʵĻ�ѧʽ�� ��
��2��B��A�ɰ�ԭ�Ӹ�����2��l��1��1�ֱ��γ����ֹ��ۻ�������Ͷ��������Ժ��ҷ�Ӧ�Ʊ���������Ҫ��ȡ�����11.2L�����������ı�������Ϊ ��ת�Ƶ�����Ϊ ����
��3��E�ĵ��ʼ��뵽C������������Ӧ��ˮ�������Һ�У�������Ӧ�����ӷ���ʽ�� ��
��4�������Ƚ�D��E������ǿ����һ��ʵ�鷽����
��
����������Ϣ�ش��������⣺
��1��DԪ�������ڱ��е�λ����
��2��B��A�ɰ�ԭ�Ӹ�����2��l��1��1�ֱ��γ����ֹ��ۻ�������Ͷ��������Ժ��ҷ�Ӧ�Ʊ���������Ҫ��ȡ�����11.2L�����������ı�������Ϊ
��3��E�ĵ��ʼ��뵽C������������Ӧ��ˮ�������Һ�У�������Ӧ�����ӷ���ʽ��
��4�������Ƚ�D��E������ǿ����һ��ʵ�鷽����
���㣺λ�ýṹ���ʵ����ϵӦ��
ר�⣺Ԫ����������Ԫ�����ڱ�ר��
������A��B��C��D��E���Ƕ�����Ԫ�أ�ԭ��������������C��B�ɰ�ԭ�Ӹ�����2��l��1��1�ֱ��γ��������ӻ�������ң���CΪNa��BΪO��A��ij�ֺ��ؿ����ڿ����ϼ���������������AΪC��E�ǵؿ��к�����ߵĽ���Ԫ�أ���EΪAl��D��ԭ����������C��E֮�䣬����DΪMg���ݴ˴��⣮
���
�⣺A��B��C��D��E���Ƕ�����Ԫ�أ�ԭ��������������C��B�ɰ�ԭ�Ӹ�����2��l��1��1�ֱ��γ��������ӻ�������ң���CΪNa��BΪO��A��ij�ֺ��ؿ����ڿ����ϼ���������������AΪC��E�ǵؿ��к�����ߵĽ���Ԫ�أ���EΪAl��D��ԭ����������C��E֮�䣬����DΪMg��
��1��DΪMg��λ��Ԫ�����ڱ��е������ڵڢ�A�壬Na��O��1��1�γ����ӻ������ң�����ΪNa2O2��
�ʴ�Ϊ���������ڵڢ�A�壻Na2O2��
��2����ΪCO2����ΪCO��CO2��Na2O2��Ӧ�Ʊ����������ݷ���ʽ2Na2O2+2CO2=2Na2CO3+O2��ÿ���ɱ����22.4L������������CO2������Ϊ88g������ת��2mol��������Ҫ��ȡ�����11.2L������������CO2������Ϊ44g��ת�Ƶ�����ΪNA��
�ʴ�Ϊ��44g��NA��
��3��C������������Ӧ��ˮ�������ҺΪNaOH����Al��Ӧ�����ӷ�ӦΪ2Al+2OH-+2H2O=2AlO2-+3H2����
�ʴ�Ϊ��2Al+2OH-+2H2O=2AlO2-+3H2����
��4�����ݽ�������ˮ�ķ�Ӧ��ȷ�������Ļ����ԣ������ʵ��Ϊþ����ˮ���Է�Ӧ����������þ����������������ˮ����Ӧ��
�ʴ�Ϊ��þ����ˮ���Է�Ӧ����������þ����������������ˮ����Ӧ��
��1��DΪMg��λ��Ԫ�����ڱ��е������ڵڢ�A�壬Na��O��1��1�γ����ӻ������ң�����ΪNa2O2��
�ʴ�Ϊ���������ڵڢ�A�壻Na2O2��
��2����ΪCO2����ΪCO��CO2��Na2O2��Ӧ�Ʊ����������ݷ���ʽ2Na2O2+2CO2=2Na2CO3+O2��ÿ���ɱ����22.4L������������CO2������Ϊ88g������ת��2mol��������Ҫ��ȡ�����11.2L������������CO2������Ϊ44g��ת�Ƶ�����ΪNA��
�ʴ�Ϊ��44g��NA��
��3��C������������Ӧ��ˮ�������ҺΪNaOH����Al��Ӧ�����ӷ�ӦΪ2Al+2OH-+2H2O=2AlO2-+3H2����
�ʴ�Ϊ��2Al+2OH-+2H2O=2AlO2-+3H2����
��4�����ݽ�������ˮ�ķ�Ӧ��ȷ�������Ļ����ԣ������ʵ��Ϊþ����ˮ���Է�Ӧ����������þ����������������ˮ����Ӧ��
�ʴ�Ϊ��þ����ˮ���Է�Ӧ����������þ����������������ˮ����Ӧ��
���������⿼��λ�á��ṹ�����ʣ���ȷԪ�ص��ƶ��ǽ����Ĺؼ�������Ϥ��ѧ�����ʹ������ɣ���Ŀ�ѶȲ���

��ϰ��ϵ�д�
�����Ŀ
��12mol/L�����ᣨ��=1.19g/cm3��50mLϡ�ͳ�6mol/L�����ᣨ��=1.10g/cm3�������ˮ�����Ϊ��������
| A��50mL |
| B��50.5mL |
| C��55mL |
| D��59.5mL |
����������һ�ֱ������Ԫ�أ����Ԫ�ط����ǣ�������
| A��I | B��Cl | C��Br | D��Si |
���������ĸ����ʵ����к�ԭ���������ǣ�������
| A��12g 12C |
| B��1mol HCl |
| C��0.5mol CH4 |
| D��3.01��1023������� |
���л�ѧ�����У���д��ȷ���ǣ�������
| A����ϩ�Ľṹ��ʽ��CH2CH2 |
| B��ˮ�Ľṹʽ��H-O-H |
C�������ӵĵ���ʽ��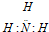 |
D����ԭ�ӵĽṹʾ��ͼ��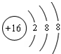 |