题目内容
10.常温下,体积相同、物质的量浓度相同的三种盐NaX、NaY、NaZ的溶液pH分别为7、9、10,则下列说法不正确的是( )| A. | 酸性强弱HX>HY>HZ | B. | 有两种盐能发生水解 | ||
| C. | 分别稀释上述三种溶液,pH均变小 | D. | 三种溶液中离子总数不相同 |
分析 相同物质的量浓度的钠盐溶液,溶液的pH越大,酸根离子的水解程度越大,其相应的酸的酸性越弱,据此解答.
解答 解:A.相同物质的量浓度的钠盐溶液,溶液的pH越大,酸根离子的水解程度越大,其相应的酸的酸性越弱,根据题意知,在三种酸HX、HY、HZ中以HX酸性相对最强HX>HY>HZ,故正确;
B.NaX、NaY、NaZ水溶液pH分别为7、9、10,说明后两种盐都是强碱弱酸盐,能水解,pH=7的钠盐不水解,故正确;
C.相同物质的量浓度的三种溶液,分别稀释,pH=7的钠盐不水解,稀释后pH不变,故C错误;
D.NaX、NaY、NaZ水溶液pH分别为7、9、10,后两种盐都是强碱弱酸盐,能水解,pH=7的钠盐不水解,溶质在溶液中的粒子数也不一定相同,三种溶液中离子总数不一定相同,故D正确;
故选C.
点评 本题考查盐类水解,明确酸的强弱与酸根离子水解程度关系是解本题关键,难度中等.

练习册系列答案
 全优点练单元计划系列答案
全优点练单元计划系列答案
相关题目
20.化学在能源开发与利用中起着重要的作用,如甲醇、乙醇、二甲醚(CH3OCH3)等都是新型燃料.
(1)乙醇是重要的化工产品和液体燃料,可以利用下列反应制取乙醇.
2CO2(g)+6H2(g)?CH3CH2OH(g)+3H2O(g)△H=a kJ/mol
在一定压强下,测得上述反应的实验数据如表.
根据表中数据分析:
①上述反应的a小于0(填“大于”或“小于”).
②在一定温度下,提高氢碳(即$\frac{n({H}_{2})}{n(C{O}_{2})}$)比,平衡常数K值不变(填“增大”、“减小”、或“不变”).
(2)催化剂存在的条件下,在固定容积的密闭容器中投入一定量的CO和H2,同样可制得乙醇(可逆反应).该反应过程中能量变化如图所示:
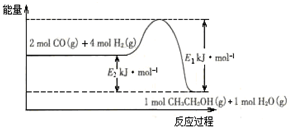
在一定温度下,向上述密闭容器中加入1mol CO、3mol H2及固体催化剂,使之反应.平衡时,反应产生的热量为Q kJ,若温度不变的条件下,向上述密闭容器中加入4mol CO、12mol H2及固体催化剂,平衡时,反应产生的热量为w kJ,则w的范围为4Q<w<2 (E2-E1).
(3)以乙醇蒸气、空气、氢氧化钠溶液为原料,石墨为电极可构成燃料电池,其工作原理与甲烷燃料电池原理相类似.该电池中负极上的电极反应式是CH3CH2OH-12e-+16OH-=2CO32-+11H2O.使用上述乙醇燃料电池电解(Pt电极)一定浓度的硫酸铜溶液通电一段时间后,向所得的溶液中加入0.1mol Cu(OH)2后恰好恢复到电解前的浓度和pH,则乙醇燃料电池在电解过程中转移电子数是0.4NA.
(1)乙醇是重要的化工产品和液体燃料,可以利用下列反应制取乙醇.
2CO2(g)+6H2(g)?CH3CH2OH(g)+3H2O(g)△H=a kJ/mol
在一定压强下,测得上述反应的实验数据如表.
| 温度/K CO2转化率% $\frac{n({H}_{2})}{n(C{O}_{2})}$ | 500 | 600 | 700 | 800 |
| 1.5 | 45% | 33% | 20% | 12% |
| 2.0 | 60% | 43% | 28% | 15% |
| 3.0 | 83% | 62% | 37% | 22% |
①上述反应的a小于0(填“大于”或“小于”).
②在一定温度下,提高氢碳(即$\frac{n({H}_{2})}{n(C{O}_{2})}$)比,平衡常数K值不变(填“增大”、“减小”、或“不变”).
(2)催化剂存在的条件下,在固定容积的密闭容器中投入一定量的CO和H2,同样可制得乙醇(可逆反应).该反应过程中能量变化如图所示:

在一定温度下,向上述密闭容器中加入1mol CO、3mol H2及固体催化剂,使之反应.平衡时,反应产生的热量为Q kJ,若温度不变的条件下,向上述密闭容器中加入4mol CO、12mol H2及固体催化剂,平衡时,反应产生的热量为w kJ,则w的范围为4Q<w<2 (E2-E1).
(3)以乙醇蒸气、空气、氢氧化钠溶液为原料,石墨为电极可构成燃料电池,其工作原理与甲烷燃料电池原理相类似.该电池中负极上的电极反应式是CH3CH2OH-12e-+16OH-=2CO32-+11H2O.使用上述乙醇燃料电池电解(Pt电极)一定浓度的硫酸铜溶液通电一段时间后,向所得的溶液中加入0.1mol Cu(OH)2后恰好恢复到电解前的浓度和pH,则乙醇燃料电池在电解过程中转移电子数是0.4NA.
5.已知4NH3+5O2?4NO+6H2O,若反应速率分别用v(NH3)、v(O2)、v(NO)、v(H2O)表示,正确的关系是( )
| A. | 4 v(NH3)=5v(O2) | B. | 5v(O2)=6v(H2O) | C. | 4v(NH3)=6 v(H2O) | D. | 4v(O2)=5 v(NO) |
15.下列实验操作或下列叙述正确的是( )
| A. | 用可见光束可以鉴别红褐色的氢氧化铁胶体和溴水,是因为溶液与胶体的本质区别是能否发生丁达尔效应 | |
| B. | 分散系是一种物质分散到另一种物质中形成的混合体系 | |
| C. | 氢氧化铁胶体具有吸附性,能吸附水中悬浮颗粒并沉降,因而常用于净水 | |
| D. | 淀粉溶液和蛋白质溶液是溶液,不可能是胶体 |
2.25℃时,水的电离达到平衡:H2O?H++OH-△H>0,下列叙述正确的是( )
| A. | 向水中加入少量固体硫酸氢钠,c(H+)增大,Kw不变 | |
| B. | 向水中加入氨水,平衡逆向移动,c(OH-)降低 | |
| C. | 向水中加入金属钠,平衡正向移动,c(H+)增大 | |
| D. | 将水加热,KW增大,pH不变 |
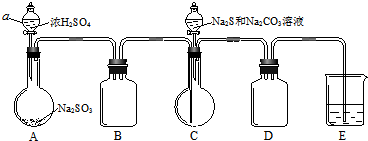
 .
.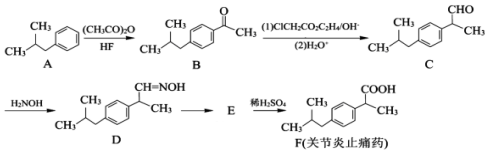
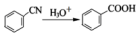 ;②
;②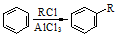 ; ③
; ③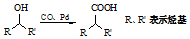 .
.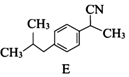 .
.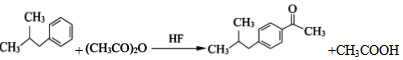 .
.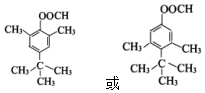 (写一种).
(写一种).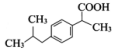 )的一种改良法是以2-甲基-1-丙醇(
)的一种改良法是以2-甲基-1-丙醇(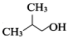 )、苯、
)、苯、 .
.