题目内容
如图是部分短周期元素原子(用字母表示)最外层电子数与原子序数的关系图.下列说法正确的是( )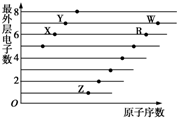

| A、X和R在同一周期 |
| B、原子半径:W>R>X |
| C、气态氢化物的稳定性:Y>X |
| D、X、Z形成的化合物中不可能含有共价键 |
考点:原子结构与元素周期律的关系
专题:元素周期律与元素周期表专题
分析:都是短周期元素,由最外层电子数与原子序数关系可知,X、Y处于第二周期,X的最外层电子数为6,故X为O元素,Y的最外层电子数为7,故Y为F元素;Z、R、W处于第三周期,最外层电子数分别为1、6、7,故Z为Na元素、R为S元素、W为Cl元素,结合对应单质、化合物的性质以及元素周期律知识解答该题.
解答:
解:都是短周期元素,由最外层电子数与原子序数关系可知,X、Y处于第二周期,X的最外层电子数为6,故X为O元素,Y的最外层电子数为7,故Y为F元素;Z、R、W处于第三周期,最外层电子数分别为1、6、7,故Z为Na元素、R为S元素、W为Cl元素,
A.X为O元素、R为S元素,二者处于同一主族,故A错误;
B.同周期自左而右,原子半径减小,电子层越多原子半径越大,故原子半径S>Cl>O,故B错误;
C.同周期自左而右,非金属性减弱,非金属性越强,气态氢化物越稳定,故气态氢化物的稳定性:F>O,故C正确;
D.X、Z形成的化合物为过氧化钠,过氧化钠中过氧根离子中氧原子之间存在非极性键,故D错误.
故选C.
A.X为O元素、R为S元素,二者处于同一主族,故A错误;
B.同周期自左而右,原子半径减小,电子层越多原子半径越大,故原子半径S>Cl>O,故B错误;
C.同周期自左而右,非金属性减弱,非金属性越强,气态氢化物越稳定,故气态氢化物的稳定性:F>O,故C正确;
D.X、Z形成的化合物为过氧化钠,过氧化钠中过氧根离子中氧原子之间存在非极性键,故D错误.
故选C.
点评:本题考查了原子结构和元素周期律的关系,同时考查学生分析问题能力,根据最外层电子数及原子序数的关系正确判断元素是解本题关键,注意整体把握元素周期表的结构,难度中等.

练习册系列答案
相关题目
如图为某含聚合物电解质薄膜的燃料电池,下列说法正确的是( )


| A、正极发生的电极反应式为:H2-2e-=2H+ |
| B、通过灯泡的电流方向是从左到右 |
| C、该聚合物电解质薄膜可通过H+的定向迁移导电 |
| D、若将灯泡换成电解饱和食盐水装置,当燃料电池生成18克水时,电解食盐水会同时产生22.4L的H2 |
在25℃时,在0.1mol/L NaX的溶液中,水电离出的OH-浓度为c1,在0.1mol?L-1的盐酸中,由水电离出的OH-浓度为c2,如果
=109,则0.1mol/L NaX的溶液的pH为( )
| c1 |
| c2 |
| A、4 | B、7 | C、10 | D、13 |
微型钮扣电池在现代生活中有广泛应用.有一种银锌电池,其电极分别是Ag2O和Zn,电解质溶液为KOH,电极反应为:
Zn+2OH--2e-=ZnO+H2O;Ag2O+H2O+2e-=2Ag+2OH-
根据上述反应式,判断下列叙述中正确的是( )
Zn+2OH--2e-=ZnO+H2O;Ag2O+H2O+2e-=2Ag+2OH-
根据上述反应式,判断下列叙述中正确的是( )
| A、在使用过程中,电池负极区溶液的pH减小 |
| B、使用过程中,电子由Ag20极经外电路流向Zn极 |
| C、Zn是正极,Ag2O是负极 |
| D、Zn电极发生还原反应,Ag2O电极发生氧化反应 |
在下列有机物中加入相应试剂和产生的现象均正确的是( )
| 选项 | 有机物 | 加入试剂 | 现象 |
| A | 苯 | 浓溴水 | 出现油状物 |
| B | 甲苯 | 酸性高锰酸钾溶液 | 紫红色变浅或消失 |
| C | 葡萄糖 | 新制氢氧化铜、加热 | 产生红色沉淀 |
| D | 溴乙烷 | 硝酸银溶液 | 产生淡黄色沉淀 |
| A、A | B、B | C、C | D、D |
下列说法中正确的是( )
| A、棉、麻、丝和毛完全燃烧都是只生成CO2和H2O |
| B、SiO2制成的玻璃纤维,由于导电能力强而被用于制造通讯光缆 |
| C、石油裂解、煤的气化、海水制镁、纤维素制火棉等过程中都包含化学变化 |
| D、固态氨基酸主要以内盐形式存在,熔点较高,不易挥发,易溶于有机溶剂 |
X、Y、Z、W 是原子序数依次递增的四种短周期元素,甲、乙、丙、丁是它们两两组合而成的化合物,且能发生甲+乙=丙+丁的反应,乙、丙、丁的化学式分别为Y2Z、YW2、ZX4,丁的结构类似甲烷,0.1 mol?L-1 甲的水溶液pH 为1(25℃).下列说法正确的是( )
| A、原子半径:W>Z>Y>X |
| B、Y 元素在周期表中的位置为第三周期第ⅡA 族 |
| C、丁的稳定性大于甲烷 |
| D、0.1 mol?L-1 甲的水溶液中,由水电离产生的c(H+)=0.1 mol?L-1 |
向含3.7g Ca(OH)2的石灰水滴加150mL 0.5mol?L-1的H3PO4溶液,待完全反应后,下列叙述正确的是( )
| A、只生成CaHPO4溶液 |
| B、有Ca3(PO4)2和CaHPO4生成 |
| C、只生成Ca(H2PO4)2溶液 |
| D、有CaHPO4和Ca(H2PO4)2生成 |
 CO2在高温高压下所形成的晶体其晶胞如图所示.该晶体的类型属于
CO2在高温高压下所形成的晶体其晶胞如图所示.该晶体的类型属于