题目内容
下列说法中正确的是( )
| A、棉、麻、丝和毛完全燃烧都是只生成CO2和H2O |
| B、SiO2制成的玻璃纤维,由于导电能力强而被用于制造通讯光缆 |
| C、石油裂解、煤的气化、海水制镁、纤维素制火棉等过程中都包含化学变化 |
| D、固态氨基酸主要以内盐形式存在,熔点较高,不易挥发,易溶于有机溶剂 |
考点:硅和二氧化硅,石油的裂化和裂解,煤的干馏和综合利用,淀粉的性质和用途,纤维素的性质和用途,氨基酸、蛋白质的结构和性质特点
专题:有机化学基础,化学应用
分析:A.组成元素只有碳和氢元素的物质或含碳、氢、氧元素的物质燃烧产物为二氧化碳和水,蛋白质含有氮元素燃烧会生成氮元素的氧化物;
B.二氧化硅具有良好的导光性;
C.化学变化是指在原子核不变的情况下,有新物质生成的变化.物理变化是指没有新物质生成的变化.化学变化和物理变化的本质区别在于是否有新物质生成;
D.氨基酸分子内的氨基与羧基反应生成内盐,熔点升高,难溶于乙醇和乙醚;
B.二氧化硅具有良好的导光性;
C.化学变化是指在原子核不变的情况下,有新物质生成的变化.物理变化是指没有新物质生成的变化.化学变化和物理变化的本质区别在于是否有新物质生成;
D.氨基酸分子内的氨基与羧基反应生成内盐,熔点升高,难溶于乙醇和乙醚;
解答:
解:A.棉麻是植物纤维,只含有C、H、O元素;丝毛是蛋白纤维,蛋白质由C、H、O、N元素组成,还可能含有S、P等,N、S、P燃烧会生成其各自的氧化物,故A错误;
B.二氧化硅具有良好的导光性,则用于制造通讯光缆,故B错误;
C.石油裂解是石油化工生产过程中,以比裂化更高的温度(700℃~800℃,有时甚至高达1000℃以上),使石油分馏产物(包括石油气)中的长链烃断裂成乙烯、丙烯等短链烃的加工过程,属于化学变化,煤的气化是煤与碳反应生成一氧化碳和氢气,属于化学变化,海水制镁通过电解熔融的氯化镁即得镁,是化学变化,纤维素和硝酸发生化学反应生成火棉,属于化学变化,故C正确;
D.氨基酸分子内的氨基与羧基反应生成内盐,熔点较高,不易挥发,溶于水,微溶于热乙醇,难溶于有机溶剂,故D错误;
故选C.
B.二氧化硅具有良好的导光性,则用于制造通讯光缆,故B错误;
C.石油裂解是石油化工生产过程中,以比裂化更高的温度(700℃~800℃,有时甚至高达1000℃以上),使石油分馏产物(包括石油气)中的长链烃断裂成乙烯、丙烯等短链烃的加工过程,属于化学变化,煤的气化是煤与碳反应生成一氧化碳和氢气,属于化学变化,海水制镁通过电解熔融的氯化镁即得镁,是化学变化,纤维素和硝酸发生化学反应生成火棉,属于化学变化,故C正确;
D.氨基酸分子内的氨基与羧基反应生成内盐,熔点较高,不易挥发,溶于水,微溶于热乙醇,难溶于有机溶剂,故D错误;
故选C.
点评:本题主要考查了生活中的有机化学,题目难度不大,注意掌握棉、麻、丝和毛的组成、石油裂解、煤的气化、海水制镁、纤维素制火棉等变化是解答的关键.

练习册系列答案
 备战中考寒假系列答案
备战中考寒假系列答案
相关题目
下列说法正确的是( )
| A、针对H7N9禽流感的扩散情况,要加强环境、个人等的消毒预防,可选用含氯消毒剂、活性银离子、酒精、双氧水等作为消毒剂,这种处理方法符合绿色化学核心 |
| B、肌红蛋白、蚕丝、过氧化氢酶、鱼油充分水解后均可得到氨基酸 |
| C、嫦娥三号月球车玉兔号在进入第二个月夜休眠前,出现了机构控制异常情况,其病因或为月尘,即月球上直径小于10微米的浮尘,月尘分散在空气中形成的分散系属于胶体 |
| D、某些铝硅酸盐形成的分子筛中有许多笼状空穴和通道,常用于分离、提纯气体或液体混合物,还可作干燥剂、离子交换剂、催化剂及催化剂载体等 |
下列说法不正确的是( )
| A、所有的蛋白质、多糖及油脂均可以水解 |
| B、氢键在形成蛋白质的二级结构和DNA的双螺旋结构中起着关键作用 |
| C、光导纤维、玻璃纤维和光电池板的主要成份均是二氧化硅 |
| D、为了减缓月饼等富脂食品变质,可在包装内放入小包装的还原铁粉 |
如图是部分短周期元素原子(用字母表示)最外层电子数与原子序数的关系图.下列说法正确的是( )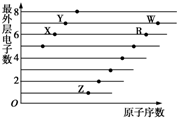

| A、X和R在同一周期 |
| B、原子半径:W>R>X |
| C、气态氢化物的稳定性:Y>X |
| D、X、Z形成的化合物中不可能含有共价键 |
 某密闭容器中,可逆反应 L(s)+G(g)?3R(g);△H>0,如图表示外界条件温度、压强的变化对上述反应的影响.下列表述正确的是( )
某密闭容器中,可逆反应 L(s)+G(g)?3R(g);△H>0,如图表示外界条件温度、压强的变化对上述反应的影响.下列表述正确的是( )| A、该反应达平衡后加入适当的催化剂可提高G的转化率 |
| B、图中的y可能是平衡混合气中G的质量分数 |
| C、达到平衡后向容器加入L,平衡向右移动,G的转化率增大 |
| D、图中的y可能是达到平衡时G的转化率 |
对下列有机反应类型的认识中,不正确的是( )
A、2CH3CH2OH+O2
| |||
B、CH3COOH+CH3CH2OH
| |||
C、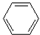 +HNO3 +HNO3
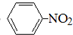 +H2O;取代反应 +H2O;取代反应 | |||
| D、CH2═CH2+Br2→CH2Br-CH2Br;加成反应 |
将0.2mol/L的醋酸钠溶液与0.1mol/L盐酸等体积混合后,溶液显酸性,则溶液中有关微粒的浓度关系正确的是( )
| A、c (Ac-)>c (Na+)>c (H+)>c (HAc) |
| B、c (Na+)+c (H+)=c (Ac-)+c (Cl-) |
| C、c (Ac-)=c (Cl-)>c (H+)>c (HAc) |
| D、c (Ac-)>c (Cl-)>c (HAc)>c(H+) |
如图为浓度各为0.1mol/L的酸HA和碱BOH的溶液中,溶质分子浓度随pH值的改变而变化的情况.下列说法中不正确的是( )
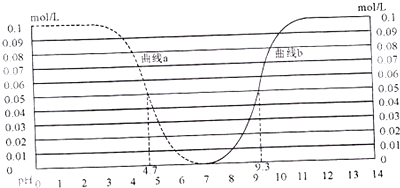

| A、曲线a代表酸HA,曲线b代表碱BOH | ||
B、在0.1mol/L的BOH溶液中,但溶液的pH从8逐渐变为11时,
| ||
| C、在0.1mol/L的NaA溶液中,若通过加少量纯HA改变溶液pH时,一定有:c(Na+)-c(OH-)=c(A-)-c(H+) | ||
| D、用等物质的量浓度的NaOH溶液和盐酸分别滴定等浓度等体积的酸HA和BOH溶液时,所消耗的NaOH溶液和盐酸的体积相同 |
在含有Cu(NO3)2、Zn(NO3)2、Fe(NO3)3、AgNO3各0.1mol的混合溶液中加入 0.1mol铁粉,充分搅拌后铁完全反应,溶液中不存在Fe3+,同时析出0.1molAg.则下列结论中不正确的是( )
| A、反应后溶液中Cu2+与Fe2+的物质的量之比为1:2 |
| B、氧化性:Ag+>Fe3+>Cu2+>Zn2+ |
| C、含Fe3+的溶液可腐蚀铜板 |
| D、1molFe可还原1molFe3+ |