题目内容
14.下列说法正确的有( )项①汽油、柴油、植物油都是碳氢化合物
②分子组成为CH2F2或C2H6O的有机物都不存在同分异构体现象
③牺牲阳极的阴极保护法是一种基于电解池原理的金属防护法
④pH=2的醋酸溶液中加入0.01mol•L-1的盐酸,溶液的pH会变小
⑤实验测定酸碱滴定曲线时,要保证整个过程测试和记录pH的间隔相同
⑥常温下pH=5的NH4Cl溶液和pH=9的NaHCO3溶液水的电离程度相同
⑦向0.1mol•L-1的醋酸和饱和硼酸溶液中滴加等浓度的碳酸钠溶液,均有气体产生
⑧AlCl3溶液,Na2SO3溶液、Fe2(SO4)3溶液加热蒸干后均不能得到溶质固体.
⑨钢铁的析氢腐蚀和吸氧腐蚀的负极反应式相同
⑩向盛有少量Mg(OH)2沉淀的试管中加入适量NH4Cl浓溶液,充分振荡后白色固体逐渐溶解,NH4+水解出的H+与Mg(OH)2电离出的OH-结合导致Mg(OH)2溶解.
| A. | 2项 | B. | 3项 | C. | 4项 | D. | 5项 |
分析 ①植物油是酯类;
②CH2F2不存在同分异构体现象;C2H6O可能为醇,还可能为醚;
③牺牲阳极的阴极保护法的原理是原电池;
④0.01mol•L-1的盐酸的pH=2;
⑤根据实验测定酸碱滴定的有关知识来回答;
⑥盐的水解促进水的电离;
⑦硼酸的酸性弱于碳酸;
⑧Fe2(SO4)3溶液加热蒸干后得硫酸铁固体;
⑨钢铁的析氢腐蚀和吸氧腐蚀的负极反应均为铁放电;
⑩氢氧化镁电离的氢氧根离子可与铵根离子反应.
解答 ①植物油是酯类,含有氧元素,故不是烃,即不是碳氢化合物,故错误;
②CH2F2不存在同分异构体现象;C2H6O可能为乙醇,还可能为二甲醚,基存在同分异构体,故错误;
③牺牲阳极的阴极保护法的原理是原电池,而非电解池,故错误;
④0.01mol•L-1的盐酸的pH=2,和醋酸溶液的酸性相同,故两溶液混合后溶液的pH不变,故错误;
⑤实验测定酸碱滴定曲线时,要保证整个过程测试和记录pH的间隔不一定相同,注意记录颜色突变过程所消耗的碱的量是关键,故错误;
⑥盐的水解促进水的电离,而常温下pH=5的NH4Cl溶液和pH=9的NaHCO3溶液中水电离出的氢离子和氢氧根的浓度均为10-5mol/L,故水的电离程度相同,故正确;
⑦硼酸的酸性弱于碳酸,故向硼酸溶液中加入碳酸钠溶液后,无气体生成,故错误;
⑧AlCl3溶液,Na2SO3溶液蒸干后分别得到氢氧化铝和硫酸钠固体,而Fe2(SO4)3溶液加热蒸干后得硫酸铁固体,故错误;
⑨钢铁的析氢腐蚀和吸氧腐蚀的负极反应均为铁放电:Fe-2e-=Fe2+,即负极反应式相同,故正确;
⑩氢氧化镁电离的氢氧根离子可与氯化铵溶液中的铵根离子反应,导致Mg(OH)2的溶解平衡右移而逐渐溶解,而不是NH4+水解出的H+与Mg(OH)2电离出的OH-结合的原因,故错误.
故选A.
点评 本题综合考查了金属的腐蚀和防护、有机物的元素组成和盐类水解的应用,综合性较强但难度不大,应注意的是向氢氧化镁中加入氯化铵溶液后氢氧化镁逐渐溶解的原理.

①Al ②Al2O3 ③Al(OH)3 ④NaHCO3 ⑤(NH4)2CO3.
| A. | ①②③④⑤ | B. | ②③④⑤ | C. | ①③④ | D. | ①②④⑤ |
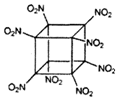 科学家研制出的八硝基立方烷(结构如图所示,碳原子未画出)是一种新型高能炸药,爆炸分解得到无毒、稳定的气体.下列说法错误的是( )
科学家研制出的八硝基立方烷(结构如图所示,碳原子未画出)是一种新型高能炸药,爆炸分解得到无毒、稳定的气体.下列说法错误的是( )| A. | 分子中C、N间形成极性共价键 | B. | 1mol该分子中含8mol-NO2 | ||
| C. | 该物质既有氧化性又有还原性 | D. | 该物质爆炸产物是NO2、CO2、H2O |
| A. | 用氨水吸收过量的二氧化硫:NH3•H2O+SO2═HSO3-+NH4+ | |
| B. | 用过氧化氢从酸化的海带灰浸出液中提取碘:2I-+H2O2+2H+═I2+2H2O | |
| C. | 向NH4Al(SO4)2溶液中滴入Ba(OH)2溶液恰好使SO42-完全沉淀:2Ba2++Al3++2SO42-+4OH-═AlO2-+2BaSO4↓+2H2O | |
| D. | 向含0.1mol•L-1Na2CO3和0.2mol•L-1NaOH的混合溶液中加入等体积的0.15mol•L-1的硫酸:CO32-+3H++2OH-═2H2O+HCO3- |
| A. | 铁表面镀锌可增强其抗腐蚀性 | |
| B. | 为防止月饼等富脂食品氧化变质,常在包装袋中放入生石灰 | |
| C. | “青蒿一握,以水二升渍,绞取汁”,上述对青篙素的提取过程属于物理变化 | |
| D. | 含重金属离子的电镀废液不能随意排放 |
 .
.