题目内容
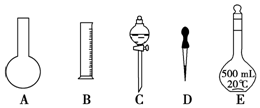
9.下列实验装置或操作与微粒的大小无直接关系的是( )| A. |  | B. |  | C. |  | D. |  |
分析 浊液、胶体、溶液的本质区别是分散质粒子的大小不同,悬浊液的分散质粒子不能通过滤纸,浊液的分散质粒子不能透过滤纸,胶体、溶液的分散质粒子能透过滤纸;胶体和浊液的分散质粒子不能透过半透膜,溶液的分散质粒子能透过半透膜;
胶体微粒能对光线散射,产生丁达尔效应,而溶液中的离子很小,不能产生丁达尔效应;
萃取利用一种溶质在两种溶剂中的溶解度不同进行分离,与物质微粒大小无直接关系,以此来解答.
解答 解:A.悬浊液的分散质粒子不能通过滤纸,过滤利用了分散质粒子的大小进行分离,故A不选;
B.胶体的分散质粒子不能透过半透膜,溶液的分散质粒子能透过半透膜,渗析利用了分散质粒子的大小进行分离,故B不选;
C.萃取利用一种溶质在两种溶剂中的溶解度不同进行分离,与物质微粒大小无直接关系,故C选;
D.胶体微粒能对光线散射,产生丁达尔效应,而溶液中的离子很小,不能产生丁达尔效应,丁达尔效应与分散质粒子的大小有关,故D不选;
故选C.
点评 本题考查胶体的性质,为高频考点,题目难度不大,把握分散系的根本区别为解答的关键,注意掌握胶体的性质,试题侧重分析与应用能力的考查.

练习册系列答案
相关题目
19.下列各个装置中能组成原电池的是( )
| A. |  | B. |  | C. | 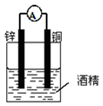 | D. |  |
17.2016年10月17日,我国神舟11号飞船发射在即,长征三号丙型运载火箭开始加注燃料.长征三号丙型火箭第一级和第二级采用偏二甲肼(UDMH)和N2O4为动力源,反应方程式为:(CH3)2N2H2+2N2O4=2CO2+4H2O+3N2,关于该反应的说法中正确的是( )
| A. | 该反应不是氧化还原反应 | B. | 氮气只是氧化产物 | ||
| C. | N2O4是还原剂 | D. | N2O4是氧化剂 |
18.硅芯片是各种计算机、微电子产品的核心.工业上通过以下反应将自然界的二氧化硅转化为硅:SiO2+2C$\frac{\underline{\;高温\;}}{\;}$Si+2CO↑,下列针对该反应的分析不正确的是( )
| A. | 属于置换反应 | B. | 碳发生了还原反应 | ||
| C. | 二氧化硅是氧化剂 | D. | 24g碳充分反应生成28g硅 |
19.下列说法正确的是( )
| A. | HClO 中氯元素化合价比 HClO4 中氯元素化合价低,所以 HClO4 的氧化性强 | |
| B. | 已知①Fe+Cu2+═Fe2++Cu; ②2Fe3++Cu═2Fe2++Cu2+,则氧化性强弱顺序为:Fe3+>Cu2+>Fe2+ | |
| C. | 已知还原性 B->C->D-,反应 2C-+D2═2D-+C2 和 2C-+B2=2B-+C2 都能发生 | |
| D. | 具有强氧化性和强还原性的物质放在一起就能发生氧化还原反应 |