题目内容
1.将X气体通入BaCl2溶液,未见沉淀生成,然后通入Y气体,有沉淀生成.X,Y不可能是( )| 选项 | X | Y |
| A | SO2 | NH3 |
| B | Cl2 | CO2 |
| C | NH3 | CO2 |
| D | SO2 | Cl2 |
| A. | A | B. | B | C. | C | D. | D |
分析 A.二氧化硫、氨气水反应生成亚硫酸铵,亚硫酸铵与氯化钡反应生成亚硫酸钡沉淀;
B.氯气、二氧化碳、氯化钡不反应;
C.氨气、二氧化碳反应生成碳酸铵,碳酸铵与氯化钡反应生成 碳酸钡沉淀;
D.氯气、二氧化硫水溶液中反应生成氯化氢和硫酸,硫酸与氯化钡反应生成硫酸钡沉淀.
解答 解:A.二氧化硫、氨气水反应生成亚硫酸铵,亚硫酸铵与氯化钡反应生成亚硫酸钡沉淀,符合题意能产生沉淀,故A不选;
B.氯气、二氧化碳、氯化钡不反应,不能产生沉淀,故B选;
C.氨气、二氧化碳反应生成碳酸铵,碳酸铵与氯化钡反应生成 碳酸钡沉淀,符合题意能产生沉淀,故C不选;
D.氯气、二氧化硫水溶液中反应生成氯化氢和硫酸,硫酸与氯化钡反应生成硫酸钡沉淀,符合题意能产生沉淀,故D不选;
故选:B.
点评 本题考查了元素化合物的性质,侧重考查二氧化硫的性质,是高考常考的知识点,熟悉各物质的性质及反应发生的条件是解题的关键,题目难度不大.

练习册系列答案
相关题目
9.下列解释实验事实的平衡不正确的是( )
| 实验 | 解释 | |
| A | 100℃0.1mol/L Na2SO4溶液pH=6.2 | H2O=H++OH- |
| B | 0.1mol/L CH3COOH的pH=3 | CH3COOH?CH3COO-+H+ |
| C | 配制FeCl3溶液时加少量盐酸 | Fe3++3H2O?Fe(OH)3+3H+ |
| D | 随温度有升高,碳酸钠溶液pH增大 | CO32-+2H2O?H2CO3+2OH- |
| A. | A | B. | B | C. | C | D. | D |
16.下列有关物质分类或归纳的说法中,正确的一组是( )
①蔗糖和麦芽糖的化学式都可用C12H22O11表示,它们互为同分异构体
②聚乙烯,聚氯乙烯,纤维素都属于合成高分子
③盐酸,漂白粉,天然油脂都是混合物
④分馏,干馏,裂化都是化学变化
⑤植物油,裂化汽油都可与溴水反应.
①蔗糖和麦芽糖的化学式都可用C12H22O11表示,它们互为同分异构体
②聚乙烯,聚氯乙烯,纤维素都属于合成高分子
③盐酸,漂白粉,天然油脂都是混合物
④分馏,干馏,裂化都是化学变化
⑤植物油,裂化汽油都可与溴水反应.
| A. | ①③⑤ | B. | ②③④ | C. | ①③④ | D. | ②④⑤ |
13.工业燃烧煤、石油等化石燃料释放出大量氮氧化物(NOx)、CO2、SO2等气体,严重污染空气.对废气进行脱硝、脱碳和脱硫处理可实现绿色环保、废物利用.
Ⅰ.脱硝:已知:H2的热值为142.9KJ•g-1
N2(g)+2O2(g)=2NO2(g)△H=+133kJ•mol-1
H2O(g)=H2O(l)△H=-44kJ•mol-1
催化剂存在下,H2还原NO2生成水蒸气和其它无毒物质的热化学方程式为4H2(g)+2NO2(g)=N2(g)+4H2O(g)△H=-1100.2kJ•mol-1.
Ⅱ.脱碳:向2L密闭容器中加入2mol CO2、6mol H2,在适当的催化剂作用下,发生反应:CO2(g)+3H2(g)?CH3OH(l)+H2O(l)
(1)①该反应自发进行的条件是低温(填“低温”、“高温”或“任意温度”)
②下列叙述能说明此反应达到平衡状态的是de.
a、混合气体的平均式量保持不变 b、CO2和H2的体积分数保持不变
c、CO2和H2的转化率相等 d、混合气体的密度保持不变
e、1mol CO2生成的同时有3mol H-H键断裂
③CO2的浓度随时间(0~t2)变化如图所示,在t2时将容器容积缩小一倍,t3时达到平衡,t4时降低温度,t5时达到平衡,请画出t2~t6CO2的浓度随时间的变化.

(2)改变温度,使反应CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H<0 中的所有物质都为气态.起始温度体积相同(T1℃、2L密闭容器).反应过程中部分数据见表:
①达到平衡时,反应I、II对比:平衡常数K(I)<K(II)(填“>”、“<”或“=”下同);平衡时CH3OH的浓度c(I)<c(II).
②对反应I,前10min内的平均反应速率v(CH3OH)=0.025mol•L-1•min-1,在其它条件不变下,若30min时只改变温度为T2℃,此时H2的物质的量为3.2mol,则T1<T2(填“>”、“<”或“=”).
若30min时只向容器中再充入1mol CO2(g)和1mol H2O(g),则平衡不移动(填“正向”、“逆向”或“不”).
Ⅰ.脱硝:已知:H2的热值为142.9KJ•g-1
N2(g)+2O2(g)=2NO2(g)△H=+133kJ•mol-1
H2O(g)=H2O(l)△H=-44kJ•mol-1
催化剂存在下,H2还原NO2生成水蒸气和其它无毒物质的热化学方程式为4H2(g)+2NO2(g)=N2(g)+4H2O(g)△H=-1100.2kJ•mol-1.
Ⅱ.脱碳:向2L密闭容器中加入2mol CO2、6mol H2,在适当的催化剂作用下,发生反应:CO2(g)+3H2(g)?CH3OH(l)+H2O(l)
(1)①该反应自发进行的条件是低温(填“低温”、“高温”或“任意温度”)
②下列叙述能说明此反应达到平衡状态的是de.
a、混合气体的平均式量保持不变 b、CO2和H2的体积分数保持不变
c、CO2和H2的转化率相等 d、混合气体的密度保持不变
e、1mol CO2生成的同时有3mol H-H键断裂
③CO2的浓度随时间(0~t2)变化如图所示,在t2时将容器容积缩小一倍,t3时达到平衡,t4时降低温度,t5时达到平衡,请画出t2~t6CO2的浓度随时间的变化.

(2)改变温度,使反应CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H<0 中的所有物质都为气态.起始温度体积相同(T1℃、2L密闭容器).反应过程中部分数据见表:
| 反应时间 | CO2(mol) | H2(mol) | CH3OH(mol) | H2O(mol) | |
| 反应I 恒温恒容 | 0min | 2 | 6 | 0 | 0 |
| 10min | 4.5 | ||||
| 20min | 1 | ||||
| 30min | 1 | ||||
| 反应II 绝热恒容 | 0min | 0 | 0 | 2 | 2 |
②对反应I,前10min内的平均反应速率v(CH3OH)=0.025mol•L-1•min-1,在其它条件不变下,若30min时只改变温度为T2℃,此时H2的物质的量为3.2mol,则T1<T2(填“>”、“<”或“=”).
若30min时只向容器中再充入1mol CO2(g)和1mol H2O(g),则平衡不移动(填“正向”、“逆向”或“不”).
10.铜锌原电池(如图)工作时,下列叙述不正确的是( )
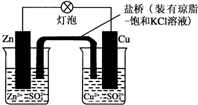

| A. | 负极反应为:Zn-2e-═Zn2+ | B. | 电池反应为:Zn+Cu2+═Zn2++Cu | ||
| C. | 在外电路中,电子从负极流向正极 | D. | 盐桥中的K+移向ZnSO4溶液 |
11.下列热化学方程式正确的是(△H的绝对值均正确)( )
| A. | 表示H2燃烧热:2H2(g)+O2(g)═2H2O1)△H=-571.6 kJ/mol | |
| B. | 表示中和热:NaOH(aq)+HCl(aq)═NaCl(aq)+H2O(1)△H=+57.3 kJ/mol | |
| C. | 表示反应热:4Al(s)+3O2(g)═2Al2O3(S)△H=-3352kJ/mol | |
| D. | 表示石墨比金刚石稳定:C(石墨)=C(金刚石)△H=-1.9 kJ/mol |
 金属冶炼和处理常涉及氧化还原反应.
金属冶炼和处理常涉及氧化还原反应.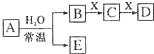 由短周期元素组成的中学常见无机物A、B、C、D、E、X 存在如在右图转化关系(部分生成物和反应条件略去),
由短周期元素组成的中学常见无机物A、B、C、D、E、X 存在如在右图转化关系(部分生成物和反应条件略去),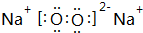 .将NaHCO3分解产生的气体(水蒸气和二氧化碳)用足量的A充分吸收得到固体甲,将甲溶于500mL 1mol/L的盐酸中,产生无色混合气体,溶液呈中性,则A的物质的量为0.25mol,混合气体在标准状况下的体积为2.8L(不考虑水蒸气的产生和其余气体的溶解).
.将NaHCO3分解产生的气体(水蒸气和二氧化碳)用足量的A充分吸收得到固体甲,将甲溶于500mL 1mol/L的盐酸中,产生无色混合气体,溶液呈中性,则A的物质的量为0.25mol,混合气体在标准状况下的体积为2.8L(不考虑水蒸气的产生和其余气体的溶解).