题目内容
11.下列热化学方程式正确的是(△H的绝对值均正确)( )| A. | 表示H2燃烧热:2H2(g)+O2(g)═2H2O1)△H=-571.6 kJ/mol | |
| B. | 表示中和热:NaOH(aq)+HCl(aq)═NaCl(aq)+H2O(1)△H=+57.3 kJ/mol | |
| C. | 表示反应热:4Al(s)+3O2(g)═2Al2O3(S)△H=-3352kJ/mol | |
| D. | 表示石墨比金刚石稳定:C(石墨)=C(金刚石)△H=-1.9 kJ/mol |
分析 A、燃烧热是在101KP时,1mol可燃物在氧气中完全燃烧生成稳定的氧化物时放出的热量;
B、酸碱中和为放热反应;
C、书写热化学方程式时,要标注物质的状态;
D、物质的能量越低,则物质越稳定.
解答 解:A、燃烧热是在101KP时,1mol可燃物在氧气中完全燃烧生成稳定的氧化物时放出的热量,此热化学方程式中氢气的计量数为2,故不能表示氢气的燃烧热,故A错误;
B、酸碱中和为放热反应,反应热应为负值,故此反应不能表示中和热,故B错误;
C、书写热化学方程式时,要标注物质的状态,4Al(s)+3O2(g)═2Al2O3(S)△H=-3352kJ/mol可以表示反应热,故C正确;
D、物质的能量越低,则物质越稳定,由于石墨比金刚石稳定,故石墨的能量更低,则转化为金刚石要吸热,反应热要为正值,故D错误.
故选C.
点评 本题考查了燃烧热、中和热和根据物质的稳定性来判断能量的高低等内容,难度不大,根据定义来分析.

练习册系列答案
 快乐小博士巩固与提高系列答案
快乐小博士巩固与提高系列答案
相关题目
2.在下列化学方程式中,不能用离子方程式:Ba2++SO42-═BaSO4↓ 来表示的是( )
| A. | Ba(NO3)2+H2SO4═BaSO4↓+2HNO3 | B. | BaCl2+Na2SO4═BaSO4↓+2NaCl | ||
| C. | Ba(OH)2+K2SO4═BaSO4↓+2KOH | D. | Ba(OH)2+H2SO4═BaSO4↓+2H2O |
6.下列各组微粒的立体构型相同的是( )
| A. | CO2与SO2 | B. | CH4与CCl4 | C. | NH3与BF3 | D. | H3O+与SO3 |
3.下列各组离子,能在指定溶液中大量共存的是( )
| A. | 无色溶液中:Na+、MnO4-、CO32-、Cl- | |
| B. | 能使紫色石蕊试剂变红的溶液中:OH-、K+、Ba2+、Na+ | |
| C. | 透明的酸性溶液中:Fe3+、Mg2+、Cl-、NO3- | |
| D. | pH=1的溶液中:NH4+、Fe2+、Cl-、NO3- |
20.下列有关说法正确的是( )
| A. | 常温下,pH=8的碱性溶液中不可能存在H2CO3分子 | |
| B. | 常温下,pH均为5的盐酸与氯化铵溶液中,水的电离程度相同 | |
| C. | 0.1mol/LCH3COOH溶液加水稀释,溶液的pH和CH3COOH的电离度均增大 | |
| D. | 将BaCl2溶液滴入含酚酞的Na2CO3溶液,红色褪去,说明BaCl2溶液显酸性 |
1.维生素C的结构简式如图,有关它的叙述错误的是( )
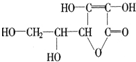

| A. | 是一个环状的酯类化合物 | B. | 易起加成及氧化反应 | ||
| C. | 可以溶解于水 | D. | 在碱性溶液中能稳定地存在 |

 ,写出B的化学式:Fe3O4,写出C的化学式:Al2O3,主要成分是J的矿石的名称:赤铁矿.
,写出B的化学式:Fe3O4,写出C的化学式:Al2O3,主要成分是J的矿石的名称:赤铁矿.


