题目内容
4.将等物质的量的Na2O和Na2O2分别投入到足量且等质量的水中,得到溶质的物质的量浓度分别为C1和C2的两种溶液,则C1和C2的关系是( )| A. | C1=C2 | B. | C1>C2 | C. | C1<C2 | D. | 无法确定 |
分析 由题意知Na2O和Na2O2物质的量相等且由方程式易知,Na2O2放在溶液中增加的质量为Na2O2中的Na2O部分,由此可知两溶液的质量相同,则C1=C2.
解答 解:反应方程式为:Na2O+H2O=2NaOH,2Na2O2+2H2O=4NaOH+O2↑,
设物质的量都为1mol,则
Na2O+H2O=2NaOH
1mol 2mol
2Na2O2+2H2O=4NaOH+O2↑
1mol 2mol
由方程式可知,生成溶质的物质的量相等,则两溶液溶质的物质的量浓度相等.
故选A.
点评 本题考查溶液浓度的计算,为高频考点,侧重于学生的分析、计算能力的考查,题目难度中等,注意本题根据反应的化学方程式进行定量计算.

练习册系列答案
 暑假衔接培优教材浙江工商大学出版社系列答案
暑假衔接培优教材浙江工商大学出版社系列答案 欣语文化快乐暑假沈阳出版社系列答案
欣语文化快乐暑假沈阳出版社系列答案
相关题目
14.如图装置能达到对应实验目的是( )
| A. |  收集氢气 | B. |  分离碘和泥沙 | ||
| C. |  分离水和四氯化碳 | D. |  实验室制取蒸馏水 |
12.常温下,下列说法正确的是( )
| A. | 0.1 mol/L的NaHA溶液pH=5,则溶液:c(HA-)>c(H+)>c(A2-)>c(H2A) | |
| B. | 等体积、等物质的量浓度的NaCl(aq) 微粒种类大于NaClO(aq)中微粒种类 | |
| C. | pH=3的硫酸溶液中水的电离程度大于pH=11的氨水溶液中水的电离程度 | |
| D. | 体积相同的0.1 mol/L氨水和0.1 mol/L NaOH溶液中和盐酸的能力后者大 |
9.现有四份体积、浓度均相等的AgNO3溶液,分别与等物质的量浓度的下列溶液恰好完全反应,所需溶液体积最小的是( )
| A. | ZnCl2溶液 | B. | NaCl溶液 | C. | CaCl2溶液 | D. | AlCl3溶液. |
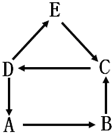 A、B、C、D、E为初中化学常见物质,A是单质,其余为化合物.E可用于检验气体B,它们之间有如图所示的转化关系(“→”表示生成,部分反应物、生成物、反应条件已省略).回答下列问题:
A、B、C、D、E为初中化学常见物质,A是单质,其余为化合物.E可用于检验气体B,它们之间有如图所示的转化关系(“→”表示生成,部分反应物、生成物、反应条件已省略).回答下列问题: