题目内容
14.乙醇是生活中常见的有机物,能进行如图所示的多种反应,A、C都是有机物.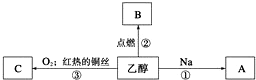
写出下列反应的化学方程式.
①:2CH3CH2OH+2Na-→2CH3CH2ONa+H2↑;
②:CH3CH2OH+3O2$\frac{\underline{\;点燃\;}}{\;}$2CO2+3H2O;
③:2CH3CH2OH+O2$→_{△}^{Cu}$2CH3CHO+2H2O.
分析 根据题中转化关系,乙醇与氧气在铜作催化剂的条件下被氧化成C为CH3CHO,乙醇与钠反应生成A为CH3CH2ONa,乙醇点燃生成B为CO2,据此答题.
解答 解:根据题中转化关系,乙醇与氧气在铜作催化剂的条件下被氧化成C为CH3CHO,乙醇与钠反应生成A为CH3CH2ONa,乙醇点燃生成B为CO2,反应①的化学方程式为2CH3CH2OH+2Na-→2CH3CH2ONa+H2↑,反应②的化学方程式为CH3CH2OH+3O2$\frac{\underline{\;点燃\;}}{\;}$2CO2+3H2O,反应③的化学方程式为2CH3CH2OH+O2$→_{△}^{Cu}$2CH3CHO+2H2O,
故答案为:2CH3CH2OH+2Na-→2CH3CH2ONa+H2↑;CH3CH2OH+3O2$\frac{\underline{\;点燃\;}}{\;}$2CO2+3H2O;2CH3CH2OH+O2$→_{△}^{Cu}$2CH3CHO+2H2O.
点评 本题考查有机物推断,涉及醇、醛的性质与转化,难度不大,有利于基础知识的巩固.

练习册系列答案
相关题目
4.将等物质的量的Na2O和Na2O2分别投入到足量且等质量的水中,得到溶质的物质的量浓度分别为C1和C2的两种溶液,则C1和C2的关系是( )
| A. | C1=C2 | B. | C1>C2 | C. | C1<C2 | D. | 无法确定 |
2.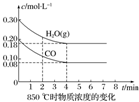 已知:CO(g)+H2O(g)?CO2(g)+H2(g)△H=Q,其平衡常数随温度变化如下表所示:
已知:CO(g)+H2O(g)?CO2(g)+H2(g)△H=Q,其平衡常数随温度变化如下表所示:
请回答下列问题:
(1)上述反应的化学平衡常数表达式为$\frac{c(C{O}_{2})×c({H}_{2})}{c(CO)×c({H}_{2}O)}$.该反应的Q<0(填“>”或“<”).
(2)850℃时在体积为10L的反应器中,通入一定量的CO和H2O(g),发生上述反应,CO和H2O(g)的物质的量浓度变化如图所示,则0~4min时平均反应速率v(CO)=0.03mol/(L•min).
(3)若在500℃时进行.且CO、H2O(g)的起始浓度均为0.020mol•L-1,该条件下,CO的最大转化率为75%.
(4)若在850℃时进行,设起始时CO和H2O(g)共为1mol,其中H2O(g)的体积分数为x,平衡时CO的转化率为y,试推导y与x之间的关系x=y.
 已知:CO(g)+H2O(g)?CO2(g)+H2(g)△H=Q,其平衡常数随温度变化如下表所示:
已知:CO(g)+H2O(g)?CO2(g)+H2(g)△H=Q,其平衡常数随温度变化如下表所示:| 温度/℃ | 400 | 500 | 850 |
| 平衡常数 | 9.94 | 9 | 1 |
(1)上述反应的化学平衡常数表达式为$\frac{c(C{O}_{2})×c({H}_{2})}{c(CO)×c({H}_{2}O)}$.该反应的Q<0(填“>”或“<”).
(2)850℃时在体积为10L的反应器中,通入一定量的CO和H2O(g),发生上述反应,CO和H2O(g)的物质的量浓度变化如图所示,则0~4min时平均反应速率v(CO)=0.03mol/(L•min).
(3)若在500℃时进行.且CO、H2O(g)的起始浓度均为0.020mol•L-1,该条件下,CO的最大转化率为75%.
(4)若在850℃时进行,设起始时CO和H2O(g)共为1mol,其中H2O(g)的体积分数为x,平衡时CO的转化率为y,试推导y与x之间的关系x=y.
19.硫有多种单质.S(单斜)和S(正交)是其中的两种同素异形体.已知:
①S(单斜,s)+O2(g)═SO2(g)△H1=-297.16kJ•mol-1
②S(正交,s)+O2(g)═SO2(g)△H2=-296.83kJ•mol-1
③S(单斜,s)═S(正交,s)△H3
下列说法不正确的是( )
①S(单斜,s)+O2(g)═SO2(g)△H1=-297.16kJ•mol-1
②S(正交,s)+O2(g)═SO2(g)△H2=-296.83kJ•mol-1
③S(单斜,s)═S(正交,s)△H3
下列说法不正确的是( )
| A. | △H3<0 | |
| B. | 正交硫比单斜硫稳定 | |
| C. | 单斜硫转化为正交硫是吸热反应 | |
| D. | 质量相等时,单斜硫能量比正交硫能量高 |
6.下列有关物质的分类正确的是( )
| A. | 混合物:空气、矿泉水、水银 | B. | 酸性氧化物:、CO2、SO2、CO | ||
| C. | 盐:醋酸钠、氯化铵、纯碱 | D. | 弱电解质:CH3COOH、H2O、NH3 |
4.25℃时,下列溶液中微粒间的物质的量浓度关系正确的是( )
| A. | 0.1 mol•L-1(NH4)2SO4溶液:(NH4+)>c(S042-)>c(H+)>(0H-) | |
| B. | 浓度均为0.1 mol•L-1的Na2CO3和NaHCO3等体积混合后的溶液:(Na+)>c(CO32-)>c(HCO3-)>(0H-) | |
| C. | 浓度均为0.1 mol•L-1NH3•H2O和NH4Cl等体积混合后的溶液:c(Cl-)>c(NH4+)>c(NH3•H2O) | |
| D. | 0.1 mol•L-1(Na)2S溶液:(0H-)=c(H+)+c(HS-)+c(H2S) |