题目内容
1.常温下,下列各组离子在指定溶液中一定能大量共存的是( )①pH=0的溶液:Na+、C2O42-、MnO4-、SO42-
②pH=11的溶液中:CO32-、Na+、AlO2-、NO3-、S2-、SO32-
③水电离的H+浓度c(H+)=10-12mol•L-1的溶液中:Cl-、CO32-、NO3-、NH4+、SO32-
④加入Mg能放出H2的溶液中:Mg2+、NH4+、Cl-、K+、SO42-
⑤使石蕊变红的溶液中:Fe2+、MnO4-、NO3-、Na+、SO42-
⑥中性溶液中:Fe3+、Al3+、NO3-、I-、Cl-、S2-.
| A. | ①③⑤ | B. | ②③⑥ | C. | ②④ | D. | ①④⑤ |
分析 ①pH=0的溶液,显酸性,离子之间发生氧化还原反应;
②pH=11的溶液,显碱性;
③水电离的H+浓度c(H+)=10-12mol•L-1的溶液,为酸或碱溶液;
④加入Mg能放出H2的溶液,显酸性;
⑤使石蕊变红的溶液,显酸性,离子之间发生氧化还原反应;
⑥中性溶液不能大量存在Fe3+,且离子之间氧化还原反应或相互促进水解.
解答 解:①pH=0的溶液中H+、C2O42-、MnO4-发生氧化还原反应,不能共存,故错误;
②pH=11的溶液,显碱性,该组离子之间不反应,可大量共存,故正确;
③水电离的H+浓度c(H+)=10-12mol•L-1的溶液,酸溶液中不能大量存在CO32-、SO32-,碱溶液中不能大量存在NH4+,故错误;
④加入Mg能放出H2的溶液,显酸性,该组离子之间不反应,可大量共存,故正确;
⑤使石蕊变红的溶液中Fe2+、MnO4-、H+发生氧化还原反应,不能共存,故错误;
⑥中性溶液不能大量存在Fe3+,且Fe3+、I-发生氧化还原反应,Al3+、S2-相互促进水解,不能共存,故错误;
故选C.
点评 本题考查离子的共存,为高频考点,把握习题中的信息及常见离子之间的反应为解答的关键,侧重复分解反应、氧化还原反应、水解反应的离子共存考查,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
11.化学与材料、生活和环境密切相关.下列有关说法中正确的是( )
| A. | 侯氏制碱法是先将CO2通入饱和NaCl溶液后,再通入NH3 | |
| B. | 新型材料聚酯纤维、光导纤维都属于有机高分子材料 | |
| C. | PM2.5是指大气中直径≤2.5×10-6m的颗粒物(气溶胶),可通过加水吸收后再利用过滤的方法分离PM2.5微粒和可溶性吸附物 | |
| D. | “神十”航天服是由碳化硅陶瓷和碳纤维复合而制成的,它是一种新型无机非金属材料 |
12.有A、B、C、D、E五种金属元素.在相同条件下,B元素的最高价氧化物对应水化物的碱性比A的弱;B、C与硫酸构成的原电池中B为负极;D单质可以与冷水剧烈反应并放出氢气;A、B、C、E四种单质分别投入盐酸中,只有E不放出氢气.则五种金属元素的金属性由强到弱的顺序为( )
| A. | D>B>A>C>E | B. | D>A>B>C>E | C. | A>B>C>E>D | D. | D>E>B>A>C |
9.下列说法正确的是( )
| A. | 含有一个苯环,对位有两个不同的取代基,且取代基均为丁基的结构有6种 | |
| B. | 若两种二肽互为同分异构体,则二者的水解产物-定不相同 | |
| C. | 芳香族化合物A的分子式为C7H6O2,其中属于芳香族化食物的结构有4种 | |
| D. | 某有机物的结构简式为 ,该有机物通过消去反应脱去1 molHCl时,能得到6种不同产物(不考虑立体异构) ,该有机物通过消去反应脱去1 molHCl时,能得到6种不同产物(不考虑立体异构) |
16. 有多种同分异构体,其中属于酯类且结构中含苯环的同分异构体有( )
有多种同分异构体,其中属于酯类且结构中含苯环的同分异构体有( )
 有多种同分异构体,其中属于酯类且结构中含苯环的同分异构体有( )
有多种同分异构体,其中属于酯类且结构中含苯环的同分异构体有( )| A. | 3种 | B. | 4种 | C. | 5种 | D. | 6种 |
6.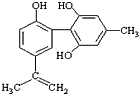 体育竞技中服用兴奋剂既有失公平,也败坏了体育道德.某种兴奋剂的结构简式如图所示.有关该物质的说法中,正确的是( )
体育竞技中服用兴奋剂既有失公平,也败坏了体育道德.某种兴奋剂的结构简式如图所示.有关该物质的说法中,正确的是( )
 体育竞技中服用兴奋剂既有失公平,也败坏了体育道德.某种兴奋剂的结构简式如图所示.有关该物质的说法中,正确的是( )
体育竞技中服用兴奋剂既有失公平,也败坏了体育道德.某种兴奋剂的结构简式如图所示.有关该物质的说法中,正确的是( )| A. | 滴入酸性高锰酸钾溶液振荡,紫色褪去,能证明其结构中存在碳碳双键 | |
| B. | 1mol该物质分别与浓溴水和H2反应时最多消耗溴水和H2分别为4mol和7mol | |
| C. | 该物质与苯酚属于同系物,遇FeCl3溶液呈紫色 | |
| D. | 该分子中的所有碳原子不可能共平面 |
13.下列说法不正确的是( )
| A. | 电解池的反应属于自发过程 | |
| B. | 化学反应热效应数值与参加反应的物质多少有关 | |
| C. | 化学反应过程中的能量变化除了热能外,也可以是光能、电能等 | |
| D. | 热化学方程式中的化学计量数只表示物质的量,可以是分数 |
10.下列有关性质的比较,不能用元素周期律解释的是( )
| A. | 酸性:H2CO3>H2SiO3 | B. | 非金属性:O>S | ||
| C. | 碱性:NaOH>Al(OH)3 | D. | 热稳定性:K2CO3>KHCO3 |
11.下列金属中,其离子溶于水中不会造成水体污染的是( )
| A. | 铅 | B. | 铬 | C. | 镉 | D. | 镁 |